Chapitre 105 – Néphroblastome et neuroblastome de l’enfant
Plan de chapitre
ITEM 297 – Cancer de l’enfant : particularités épidémiologiques, diagnostiques et thérapeutiques
I. Généralités
– A. Néphroblastome
– B. Neuroblastome
II. Stratégie d’exploration en imagerie
Situations de départ
- 3 Distension abdominale.
- 4 Douleur abdominale.
- 6 Hépatomégalie.
- 8 Masse abdominale.
- 13 Vomissements.
- 42 Hypertension artérielle.
- 55 Pâleur de l’enfant.
- 66 Apparition d’une difficulté à la marche.
- 68 Boiterie.
- 71 Douleur d’un membre (supérieur ou inférieur).
- 72 Douleur du rachis (cervical, dorsal ou lombaire).
- 89 Purpura/ecchymose/hématome.
- 121 Déficit neurologique sensitif et/ou moteur.
- 158 Tuméfaction cervico-faciale.
- 224 Découverte d’une anomalie abdominale à l’examen d’imagerie médicale.
- 225 Découverte d’une anomalie cervico-faciale à l’examen d’imagerie médicale.
- 227 Découverte d’une anomalie médullaire ou vertébrale à l’examen d’imagerie médicale.
- 228 Découverte d’une anomalie osseuse et articulaire à l’examen d’imagerie médicale.
- 229 Découverte d’une anomalie pelvienne à l’examen d’imagerie médicale.
Item, hiérarchisation des connaissances
ITEM 297 – Cancer de l’enfant : particularités épidémiologiques, diagnostiques et thérapeutiques
| Rang | Rubrique | Intitulé | Descriptif |
| Prévalence, épidémiologie | Particularités épidémiologiques des tumeurs malignes de l’enfant* | Prévalence des cancers, principaux cancers selon l’âge | |
| Prévalence, épidémiologie | Connaître les principales prédispositions génétiques et autres facteurs de risque aux tumeurs malignes de l’enfant* | ||
| Diagnostic positif | Connaître les circonstances et signes cliniques devant faire évoquer une tumeur cérébrale chez l’enfant* | ||
| Diagnostic positif | Connaître les circonstances et signes cliniques devant faire évoquer une tumeur abdominale chez l’enfant* | ||
| Diagnostic positif | Connaître les circonstances et signes cliniques devant faire évoquer une tumeur thoracique chez l’enfant* | ||
| Diagnostic positif | Connaître les circonstances et signes cliniques devant faire évoquer une tumeur osseuse chez l’enfant* | ||
| Examens complémentaires | Indication et objectifs des examens d’imagerie devant une situation évocatrice de cancer de l’enfant (tumeurs cérébrale, abdominale, thoracique et osseuse) | ||
I. Généralités

Les deux tumeurs solides malignes extracrâniennes les plus fréquentes de l’enfant de moins de 5 ans sont le néphroblastome (tumeur du rein) et le neuroblastome (développé à partir des dérivés de la crête neurale : médullosurrénale ou éléments du système nerveux autonome sympathique).
A. Néphroblastome

Le néphroblastome (ou tumeur de Wilms) représente à lui seul 90 % des tumeurs rénales de l’enfant. Il survient dans 5 % des cas sur un terrain génétique prédisposant et est alors volontiers multifocal et/ou bilatéral (syndrome de Beckwith-Wiedemann, syndrome de Denys-Drash, syndrome WAGR et quelques autres plus rares). Environ 10 % sont métastatiques d’emblée (poumons). Dans les formes cliniquement et radiologiquement typiques, le traitement peut être instauré sans preuve histologique (chimiothérapie néoadjuvante, néphrectomie totale élargie et traitement postopératoire adapté au stade et à la forme histologique).
B. Neuroblastome
L’origine des neuroblastomes est variable : 70 % surviennent dans le rétropéritoine (d’où parfois des problèmes de diagnostic différentiel avec les tumeurs rénales), 15 % dans le médiastin postérieur (avec une extension possible dans le canal rachidien) et plus rarement dans le cou ou le pelvis. Environ 50 % sont métastatiques au diagnostic (moelle osseuse, os et foie principalement). Le dosage des catécholamines urinaires (acide vanylmandélique, acide homovanillique et dopamine) est un marqueur diagnostique. Le traitement est réalisé selon des protocoles internationaux complexes stratifiés selon les facteurs pronostiques principaux : l’âge (meilleur pronostic si âge < 18 mois), le stade, le sous-type histologique et le profil génomique de la tumeur (mauvais pronostic des 20 % de formes avec amplification du gène MYCN).
II. Stratégie d’exploration en imagerie
Devant une masse abdominale, l’échographie est l’examen de première intention. Elle permet de déterminer l’organe dont dépend la tumeur et participe au bilan d’extension de la lésion (figures 105.1 et 105.2).
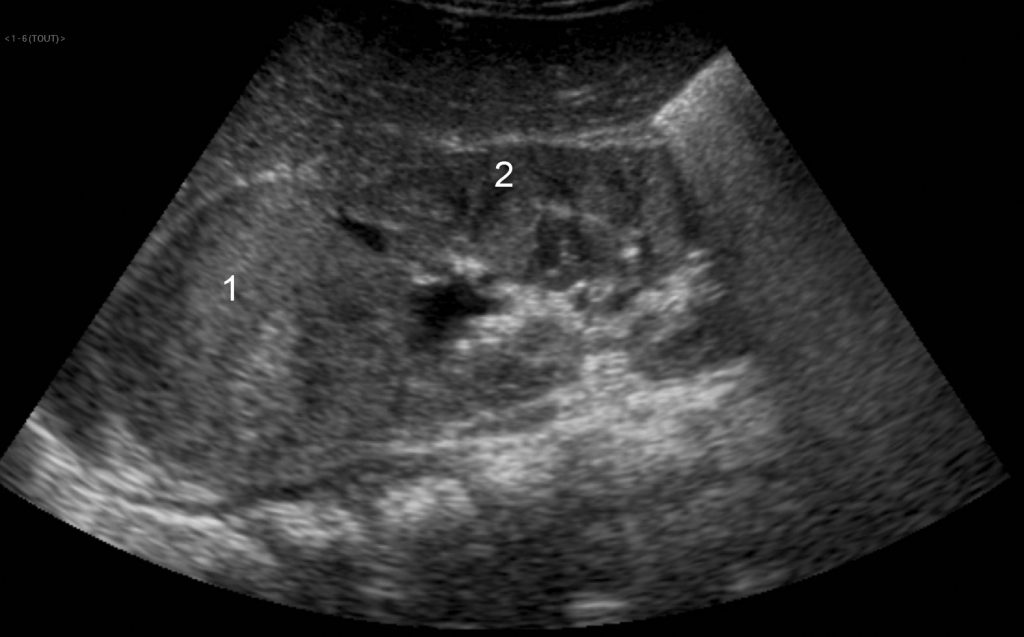

Fig. 105.1 Coupe longitudinale sur le flanc droit chez un enfant de 2 ans.
L’échographie met en évidence une masse (1) développée aux dépens du pôle supérieur du rein (2). Cette masse est d’échostructure tissulaire. L’âge de l’enfant, la localisation rénale et le caractère tissulaire suggèrent fortement le diagnostic de néphroblastome.
Source : CERF, CNEBMN, 2022.
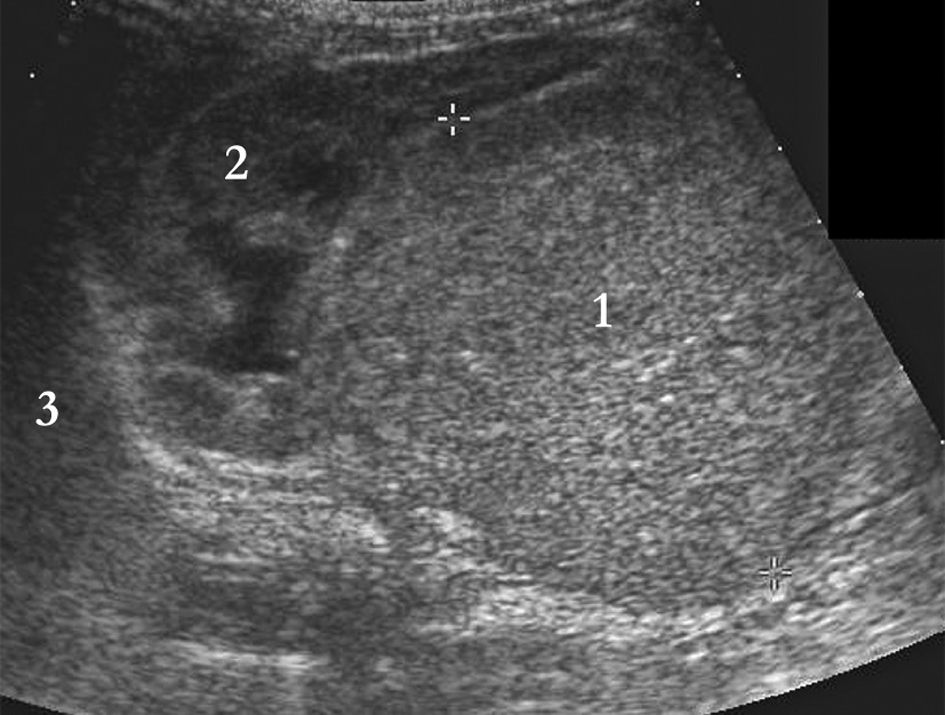

Fig. 105.2 Coupe longitudinale sur le flanc droit mettant en évidence un neuroblastome avec injection de produit de contraste.
La masse (1) est homogène, d’échostructure tissulaire, et refoule le rein droit normal (2). Un liséré hyperéchogène sépare les deux. Le foie (3) est refoulé vers le haut.
Source : CERF, CNEBMN, 2022.
Le cliché d’abdomen sans préparation n’est plus indiqué pour le diagnostic des tumeurs abdominales de l’enfant.
L’IRM ou la TDM (avec injection) précise l’origine anatomique de la tumeur (intra- ou extrarénale), ses rapports avec les organes voisins et avec les principaux vaisseaux. Elle recherche des anomalies locorégionales comme des adénopathies ou une seconde localisation (figures 105.3 et 105.4).
L’IRM est indispensable pour évaluer l’extension intracanalaire et le risque de compression médullaire en cas de neuroblastome paravertébral.
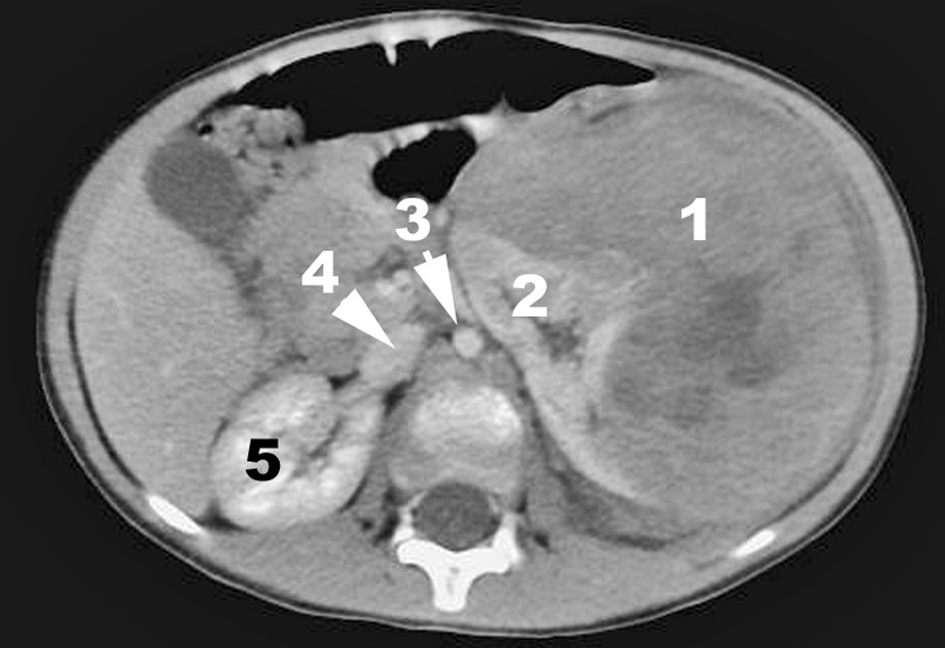

Fig. 105.3 Exemple de néphroblastome en tomodensitométrie.
La tumeur, partiellement nécrosée (1), est enchâssée dans le rein gauche (2). Autres structures : aorte (3), veine cave inférieure (4), rein droit (5).
Source : CERF, CNEBMN, 2022.
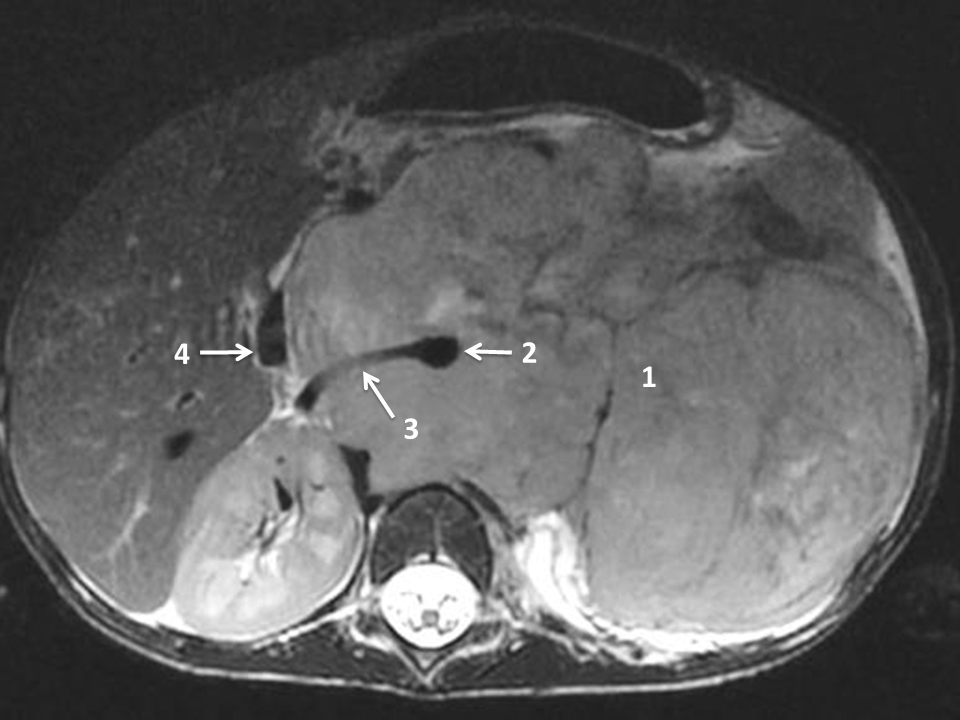

Fig. 105.4 IRM en coupe axiale et pondération T2. Volumineux neuroblastome surrénalien gauche.
La tumeur (1) infiltre le rétropéritoine médian en englobant l’aorte (2), l’artère rénale droite (3) ; la veine cave inférieure est refoulée à droite (4).
Source : CERF, CNEBMN, 2022.

La scintigraphie à la 123I-MIBG (méta-iodo-benzyl-guanidine, précurseur de la noradrénaline marqué par l’iode 123) est l’examen de référence pour le bilan d’extension initial du neuroblastome (figures 105.5 et 105.6).
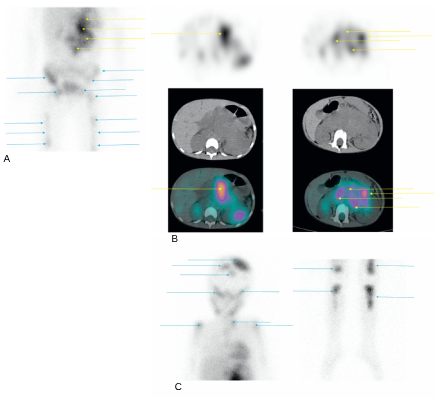

Fig. 105.5 Scintigraphie à la 123I-MIBG d’un enfant de 4 ans présentant un neuroblastome surrénalien gauche.
La volumineuse masse tumorale abdominale fixe la 123I-MIBG. Les images planaires mettent en évidence plusieurs hyperfixations du squelette en faveur de localisations secondaires. A. Image planaire, vue antérieure centrée sur l’abdomen, le bassin et les cuisses. B. images axiales tomoscintigraphiques couplées TDM centrées sur l’abdomen (flèches jaunes). C. Images planaires vue antérieure centrées sur le crâne et le thorax et sur les jambes, (flèches bleues).
Source : CERF, CNEBMN, 2022.
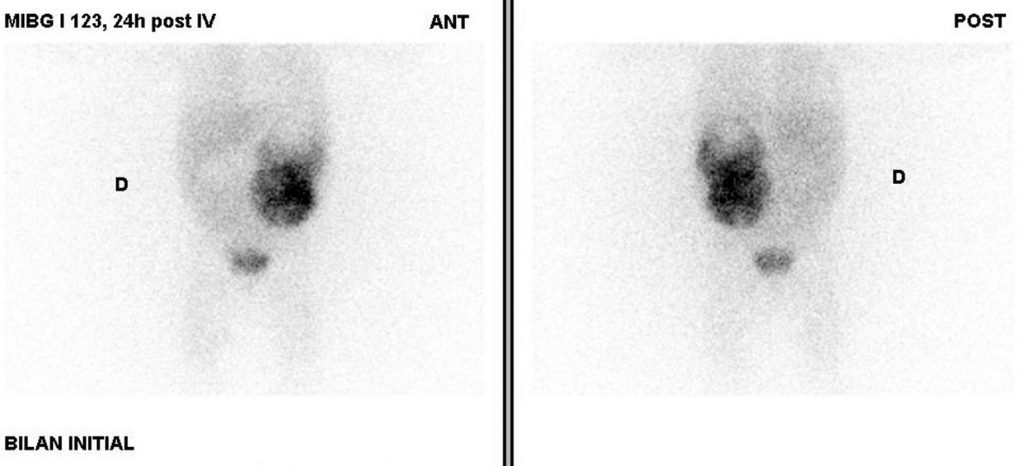

Fig. 105.6 Scintigraphie à la 123I-MIBG d’un enfant de 18 mois présentant un neuroblastome surrénalien gauche.
Le tissu tumoral fixe la 123I-MIBG, sauf dans sa partie supérieure qui est nécrosée. La vessie est visible du fait de l’élimination urinaire du traceur. Il n’y a pas de localisation secondaire, notamment sur le squelette.
Source : CERF, CNEBMN, 2022.
Points clés
- L’échographie est l’examen de première intention devant une masse abdominale.
- Le cliché d’abdomen sans préparation n’est plus indiqué pour le diagnostic des tumeurs abdominales de l’enfant.
- L’IRM ou la TDM précise l’origine anatomique de la tumeur, ses rapports avec les organes voisins et recherche des anomalies locorégionales. Elle est indispensable pour évaluer l’extension intracanalaire et le risque de compression médullaire en cas de neuroblastome paravertébral.
- La scintigraphie à la 123I-MIBG est indiquée pour le bilan d’extension initial des neuroblastomes.