Plan de chapitre
ITEM 299 – Tumeurs intracrâniennes
I. Généralités
II. Stratégie d’exploration en imagerie
III. Sémiologie
– A. Méningiome (tumeur intracrânienne extraparenchymateuse) V
– B. Glioblastome
– C. Métastases cérébrales
Situations de départ
- 118 Céphalée.
- 119 Confusion mentale/désorientation.
- 120 Convulsions.
- 121 Déficit neurologique sensitif et/ou moteur.
Item, hiérarchisation des connaissances
ITEM 299 – Tumeurs intracrâniennes
| Rang | Rubrique | Intitulé | Descriptif |
| Définition | Principaux types et localisations des tumeurs intracrâniennes* | Savoir distinguer : tumeur primitive/secondaire, de l’encéphale/des annexes, bénigne/maligne, fréquente/rare, sus-/sous-tentorielle | |
| Définition | Tumeurs primitives intracrâniennes : SNC et annexes* | Connaître la distinction entre tumeur provenant du SNC et tumeur provenant de ses annexes | |
| Définition | Connaître les principaux types histologiques des tumeurs cérébrales* | Méningiome et adénome hypophysaire, tumeurs gliales de bas grade et de haut grade (glioblastome), métastases | |
| Prévalence, épidémiologie | Tumeurs primitives intracrâniennes : différents types* | Connaître les principaux types de tumeurs primitives intracrâniennes et leur origine | |
| Diagnostic positif | Fomes et symptômes cliniques* | Connaître les principaux tableaux cliniques devant faire évoquer une tumeur intracrânienne | |
| Examens complémentaires | Connaître la stratégie d’exploration en imagerie devant une tumeur intracrânienne de l’adulte | Le scanner et l’IRM sans et avec injection permettent d’évoquer le diagnostic de tumeur mais l’IRM est plus performante pour le diagnostic et le bilan préopératoire | |
| Diagnostic positif | Tumeurs secondaires intracrâniennes : recherche du cancer primitif | Décrire la recherche systématique de cancer primitif à effectuer devant une métastase cérébrale | |
| Identifier une urgence | Savoir évoquer une HTIC, une épilepsie chez un patient porteur d’une tumeur intracérébrale* | Connaître les deux principales urgences (HTIC, épilepsie) révélant ou compliquant l’évolution d’une tumeur cérébrale | |
| Suivi et/ou pronostic | Connaître les principes de la prise en charge de l’HTIC et de l’épilepsie chez un patient porteur d’une tumeur intracérébrale* | ||
I. Généralités
Les tumeurs intracrâniennes sont soit extraparenchymateuses soit intraparenchymateuses (ou cérébrales), primitives ou secondaires (métastases cérébrales). Les tumeurs extraparenchymateuses les plus fréquentes sont les méningiomes : ce sont des tumeurs le plus souvent bénignes, à croissance lente, développées aux dépens des cellules arachnoïdiennes et implantées sur la dure-mère. Les gliomes sont les tumeurs cérébrales primitives les plus fréquentes du système nerveux central. Ils présentent un grade de malignité ; le glioblastome est un gliome de haut grade de malignité de mauvais pronostic. Les métastases cérébrales sont les plus fréquentes des tumeurs intracrâniennes et peuvent compliquer tous les cancers, notamment du poumon, du sein, du rein et du tube digestif, ainsi que les mélanomes ; elles sont souvent multiples.
II. Stratégie d’exploration en imagerie

Ces tumeurs présentent des aspects différents en imagerie mais, même si certains sont évocateurs, ils ne sont pas suffisamment spécifiques et le diagnostic de nature repose sur l’examen anatomopathologique.
Le scanner et l’IRM permettent d’évoquer le diagnostic de tumeur mais l’IRM est plus performante pour le diagnostic et le bilan préopératoire.
L’IRM doit être réalisée sans et avec injection intraveineuse de produit de contraste et permettra :
- d’évoquer le diagnostic de tumeur en mettant en évidence un processus le plus souvent expansif (avec effet de masse) ;
- de localiser ce processus en extra- ou intraparenchymateux, en sus- ou sous-tentoriel, unique ou multiple ;
- de préciser ses caractéristiques (hémorragie, œdème, prise de contraste, nécrose, calcifications) ;
- de discuter les diagnostics différentiels (notamment les abcès cérébraux dans le cas des tumeurs cérébrales) ;
- de rechercher des complications évolutives et notamment des signes d’engagement (cf. chapitre 55) ;
- de préciser ses rapports avec le parenchyme cérébral, les ventricules, les vaisseaux, l’os, etc. ;
- de répondre aux critères d’opérabilité de la tumeur (taille, localisation, nombre).
III. Sémiologie
A Méningiome (tumeur intracrânienne extraparenchymateuse)
Le diagnostic de méningiome est assez caractéristique : c’est une masse extraparenchymateuse en général adossée à la méninge, refoulant le cortex et parfois séparée de lui par du liquide cérébrospinal (figure 61.1). Une hyperostose de la voûte en regard est possible (figure 61.2). Elle présente un signal variable en T2/FLAIR mais se rehausse intensément (absence de barrière hématoencéphalique) (figures 61.1 et 61.2). L’effet de masse est variable mais un engagement est possible.
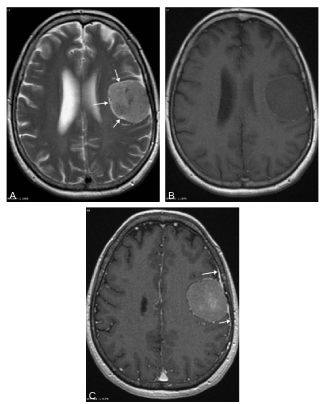

Fig. 61.1. Méningiome pariétal gauche.
Coupes axiales IRM pondérées en T2 (A), T1 (B) et T1 après injection de gadolinium (C) : masse pariétale gauche à contours bien limités, séparée du parenchyme cérébral par un liseré de liquide cérébrospinal visible en hypersignal en T2 (flèches blanches), se rehaussant de façon intense et homogène après injection (C) et associée à une prise de contraste et à un épaississement méningé (flèches blanches).
Source : CERF, CNEBMN, 2022.
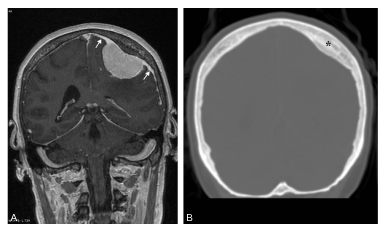

Fig. 61.2. Méningiome pariétal gauche.
Coupe frontale IRM pondérée en T1 avec injection de gadolinium (A) : masse pariétale gauche extraparenchymateuse (c’est-à-dire refoulant le cortex cérébral), prenant fortement le contraste, et associée à un épaississement méningé (flèches) avec hyperostose de la voûte crânienne au contact de la lésion (∗) sur le scanner en fenêtre osseuse (B).
Source : CERF, CNEBMN, 2022.
B. Glioblastome
Le glioblastome est une masse expansive intraparenchymateuse, hémisphérique à contours souvent mal limités, hétérogène, présentant un contingent nécrotique central (hypodense au scanner, en hypersignal en T2 et en hyposignal en T1 en IRM) et un contingent tissulaire périphérique épais et irrégulier qui prend le contraste (figure 61.3). Un œdème périlésionnel dans la substance blanche est souvent marqué (hypodensité au scanner et hypersignal en T2/FLAIR, hyposignal en T1).
La séquence en diffusion permet d’aider au diagnostic différentiel avec un abcès cérébral à pyogènes en cas de doute clinique (cf. chapitre 49).
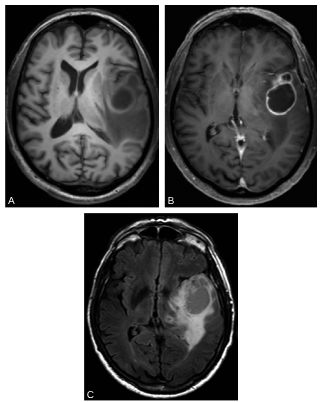

Fig. 61.3. Glioblastome temporal gauche.
IRM en coupe axiale en T1 sans injection de gadolinium (A), en T1 après injection (B) et en FLAIR (C). Masse intraparenchymateuse temporale gauche entourée d’un œdème avec effet de masse sur la ligne médiane. Elle est hétérogène, nécrotique, prend le contraste en périphérie et s’accompagne d’un œdème étendu « en doigts de gant ».
Source : CERF, CNEBMN, 2022.
C. Métastases cérébrales
Ce sont des lésions arrondies, le plus souvent multiples, prenant le contraste en anneau ou de façon nodulaire, entourées d’un œdème de la substance blanche « en doigts de gant » souvent très étendu, disproportionné par rapport à la taille de la tumeur (figure 61.4).
L’effet de masse est variable, pouvant entraîner une hydrocéphalie par compression des ventricules ou un engagement cérébral.
Des atteintes osseuses de type ostéolytique ou ostéocondensante peuvent y être associées (métastases osseuses).
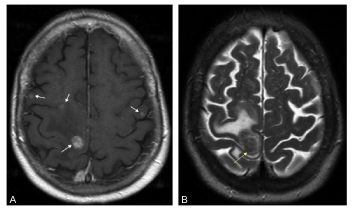
Fig. 61.4. Métastases cérébrales.
IRM. Coupe axiale en T1 après injection de gadolinium (A) : présence de quatre rehaussements nodulaires périphériques évoquant des métastases cérébrales (flèches). Coupe axiale T2 (B) : lésion parafalcorielle droite entourée d’un œdème en « doigts de gant ».
Source : CERF, CNEBMN, 2022.
Points clés
- Distinguer en imagerie (IRM) les tumeurs extraparenchymateuses des tumeurs intraparenchymateuses.
- La tumeur extraparenchymateuse la plus fréquente est le méningiome, caractérisé par une prise de contraste intense.
- Le glioblastome est une tumeur intraparenchymateuse d’aspect hétérogène avec un œdème périlésionnel (en hypersignal T2/FLAIR).
- Les métastases sont le plus souvent multiples avec une prise de contraste en anneau et un œdème périlésionnel souvent disproportionné par rapport à la taille de la tumeur.