Plan de chapitre
ITEM 207 – Opacités et masses intrathoraciques chez l’enfant et chez l’adulte
ITEM 309 – Tumeurs du poumon, primitives et secondaires
Tumeurs primitives du poumon
I. Généralités
II. Stratégie d’exploration en imagerie
– A. Bilan initial
– B. Place de la TEP-TDM au 18FDG
– C. Place de l’IRM
III. Sémiologie
Tumeurs secondaires du poumon
I. Généralités
II. Stratégie d’exploration en imagerie
V. Sémiologie
– A. Radiographie thoracique
– B. Tomodensitométrie
– C. TEP-TDM au 18FDG
Situations de départ
- 14 Émission de sang par la bouche.
- 17 Amaigrissement.
- 20 Découverte d’anomalie à l’auscultation pulmonaire.
- 21 Asthénie.
- 161 Douleur thoracique.
- 162 Dyspnée.
- 167 Toux.
- 297 Consultation de suivi en cancérologie.
- 303 Prévention/dépistage des cancers de l’adulte.
- 314 Prévention des risques liés au tabac.
Items, hiérarchisation des connaissances
ITEM 207 – Opacités et masses intrathoraciques chez l’enfant et chez l’adulte
| Rang | Rubrique | Intitulé | Descriptif |
| Diagnostic positif | Reconnaître une opacité pulmonaire chez l’enfant et l’adulte | Reconnaître une anomalie sur un ou deux poumons | |
| Diagnostic positif | Reconnaître une fracture de côte chez l’enfant et l’adulte* | ||
| Diagnostic positif | Savoir diagnostiquer un épanchement pleural liquidien chez l’enfant et l’adulte* | Diagnostiquer une pleurésie | |
| Diagnostic positif | Savoir diagnostiquer un épanchement pleural gazeux chez l’enfant et l’adulte* | Diagnostiquer un pneumothorax | |
| Diagnostic positif | Savoir diagnostiquer un syndrome alvéolaire* | Reconnaître une opacité alvéolaire et un bronchogramme aérien | |
| Diagnostic positif | Savoir diagnostiquer un syndrome interstitiel* | Reconnaître un infiltrat pulmonaire | |
| Diagnostic positif | Savoir repérer une anomalie médiastinale* | Tumeur, emphysème, élargissement aortique, cardiomégalie | |
| Diagnostic positif | Savoir diagnostiquer une atélectasie* | Diagnostiquer un trouble ventilatoire | |
| Diagnostic positif | Savoir quand demander une radiographie thoracique en urgence* | ||
| Diagnostic positif | Savoir identifier une image thymique normale sur une radiographie thoracique de face chez un nourrisson* | ||
| Diagnostic positif | Savoir identifier une image médiastinale anormale chez le nourrisson et l’enfant et prescrire un scanner thoracique* | ||
| Étiologie | Connaître les principales hypothèses diagnostiques devant une anomalie médiastinale selon la topographie chez l’enfant* | ||
ITEM 309 – Tumeurs du poumon, primitives et secondaires
| Rang | Rubrique | Intitulé | Descriptif |
| Définition | Principaux types histologiques des cancers bronchopulmonaires* | Adénocarcinome, carcinome épidermoïde, carcinome à petites cellules, métastase | |
| Prévalence, épidémiologie | Épidémiologie descriptive | Connaître l’incidence et la mortalité par cancer du poumon (absolue et relative ; France et monde ; tendances évolutives) ainsi que les principales données sociodémographiques et pronostiques à son sujet Connaître l’importance en termes de santé publique du cancer du poumon, les principaux types histologiques et la fréquence des tumeurs découvertes au stade métastatique Caractériser l’importance du tabac dans l’étiologie du cancer du poumon (en termes de risque et de modalités de toxicité) | |
| Étiologie | Connaître les principaux facteurs de risque professionnels et environnementaux* | Lister les principaux facteurs de risque (personnels et professionnels) de cancer du poumon Lister les principaux facteurs de risques (génétiques et environnementaux) de cancer du poumon | |
| Diagnostic positif | Connaître les circonstances de découvertes et les manifestations cliniques des tumeurs du poumon (y compris syndromes paranéoplasiques) | Connaître les principaux signes et situations cliniques devant faire évoquer un cancer du poumon (au stade localisé, localement avancé et métastatique) | |
| Diagnostic positif | Connaître la démarche diagnostique devant une tumeur du poumon | Lister les différentes procédures à réaliser devant la suspicion d’un cancer du poumon (examen clinique, bilan biologique, radiographie thoracique, TDM) | |
| Définition | Particularités du cancer à petites cellules* | ||
| Examens complémentaires | Connaître les examens d’imagerie et leurs indications dans l’exploration d’une tumeur primitive du poumon | ||
| Contenu multimédia | Exemple de radiographie de face d’un adénocarcinome pulmonaire | Imagerie typique | |
| Contenu multimédia | Exemple de TDM thoracique en fenêtre parenchymateuse d’une tumeur primitive du poumon | ||
| Examens complémentaires | Connaître les principales investigations à visée diagnostique d’un cancer bronchique | ||
| Prise en charge | Connaître les principes de la prise en charge d’une tumeur du poumon primitive ou secondaire* | Connaître les principales modalités thérapeutiques disponibles en oncologie thoracique | |
Tumeurs primitives du poumon
I. Généralités

Avec une survie moyenne à 5 ans de 15 % et 46 000 nouveaux cas par an, le cancer bronchique est la première cause de mortalité par cancer. Le tabagisme en est le principal facteur de risque. Le pronostic des patients est très différent selon que la tumeur peut être réséquée chirurgicalement (20 % des patients, 70 % de survie à 5 ans) ou qu’elle n’est pas résécable car localement avancée ou métastatique dès le diagnostic initial (80 % des patients, 5 à 10 % de survie à 5 ans).
Il est habituel de faire la distinction entre deux groupes de carcinomes bronchiques :
- le carcinome à petites cellules (15 % des cas), tumeur radio- et chimiosensible mais de mauvais pronostic car très aggressive ;
- le groupe des carcinomes non à petites cellules (85 % des cas), avec pour chefs de file l’adénocarcinome (55 %) et le carcinome épidermoïde (25 %).
La radiographie thoracique manque de sensibilité pour détecter les tumeurs de petite taille et ne permet pas de faire le bilan d’extension. L’imagerie TDM et TEP au 18FDG joue un rôle essentiel dans le diagnostic positif et le bilan d’extension. Le scanner permet par ailleurs de guider la réalisation des biopsies percutanées.
II. Stratégie d’exploration en imagerie
A. Bilan initial

Le bilan initial comporte un scanner thoracique et abdominal avec injection, une imagerie cérébrale (IRM ou scanner) et une TEP-TDM au 18FDG. La biopsie de la tumeur à visée diagnostique est indispensable ; elle peut se faire lors d’une fibroscopie bronchique (tumeurs proximales) ou être réalisées par un guidage scannographique. Au terme du bilan, la tumeur sera classée selon la stadification TNM (8e édition).
B. Place de la TEP-TDM au 18FDG
La TEP-TDM au 18FDG est recommandée pour caractériser les nodules pulmonaires solides de taille supérieure à ou égale à 8 mm :
une lésion non hypermétabolique doit faire l’objet d’une surveillance radiologique ;
- une lésion hypermétabolique doit faire l’objet d’un contrôle histologique, sauf si elle possède les caractéristiques d’une étiologie infectieuse ou inflammatoire.

La TEP au 18FDG est recommandée pour le bilan d’extension des cancers bronchiques non à petites cellules (CBNPC) en l’absence de localisation à distance avérée, et peut être proposée pour le bilan d’extension des carcinomes pulmonaires à petites cellules (CPPC).

La TEP au 18FDG peut par ailleurs être proposée pour évaluer la réponse tumorale aux traitements systémiques. La TEP au 18FDG est enfin recommandée en cas de suspicion de récidive des cancers bronchopulmonaires.
C. Place de l’IRM
L’IRM cérébrale est recommandée pour le bilan initial des cancers à petites cellules et est préférable pour les cancers non à petites cellules — l’alternative est le scanner injecté.

L’IRM thoracique est rarement réalisée. Sa seule indication est le bilan des tumeurs de l’apex (de Pancoast-Tobias) : elle permet d’analyser l’extension tumorale aux vaisseaux subclaviers, au plexus brachial et foramens intervertébraux, dont va dépendre la résécabilité.
Le scanner sans injection à faible dose s’installe aussi progressivement comme un outil de dépistage chez les sujets à haut risque de cancer bronchique.
III. Sémiologie
Les tumeurs primitives se présentent sous plusieurs formes :
- nodule ou masse (une masse est une lésion supérieure à 3 cm) solide, parfois excavé(e), à contours spiculés ou lobulés, irréguliers (figures 101.1 et 101.2) ;
- nodule ou masse en « verre dépoli » (peu dense) accompagné(e) ou non d’une portion solide.
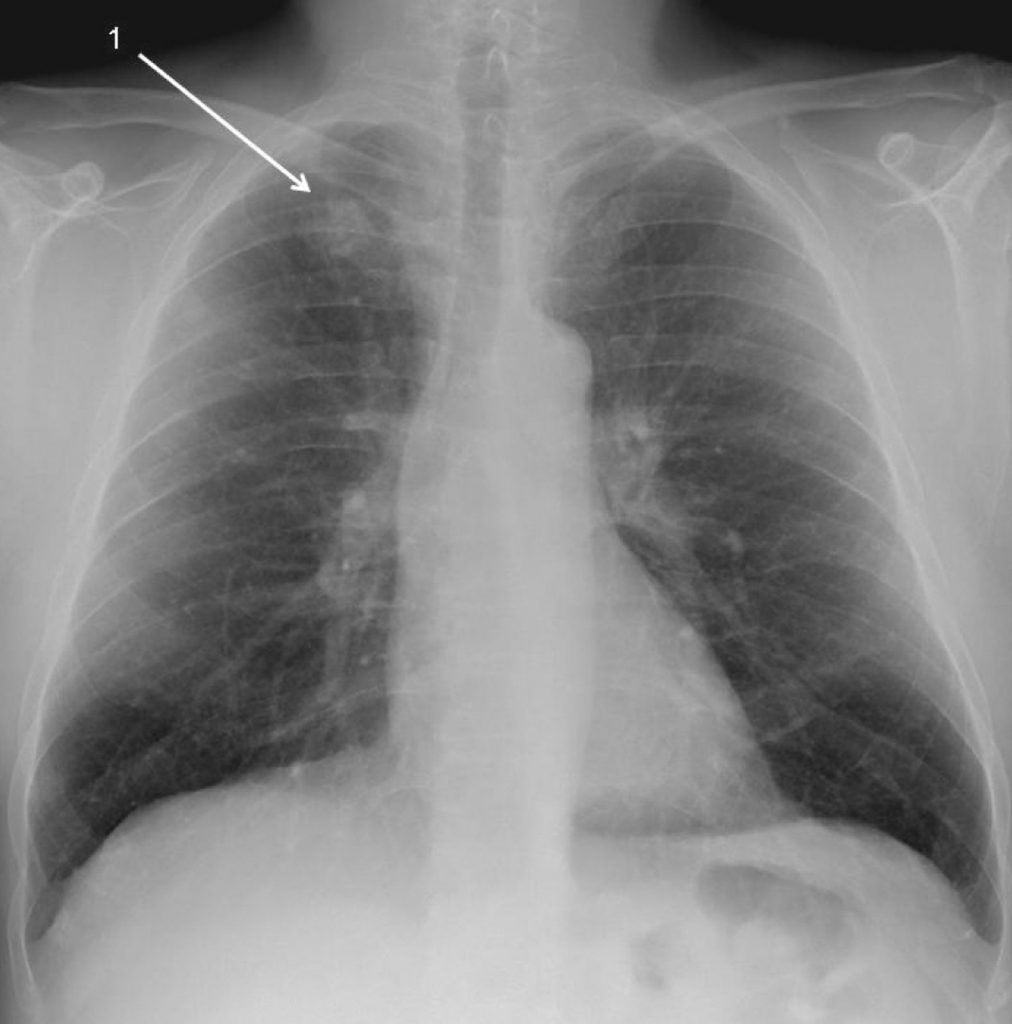
Fig. 101.1. Radiographie de face. Macronodule de l’apex pulmonaire droit (1).
Il s’agissait d’un adénocarcinome (flèche).
Source : CERF, CNEBMN, 2022.
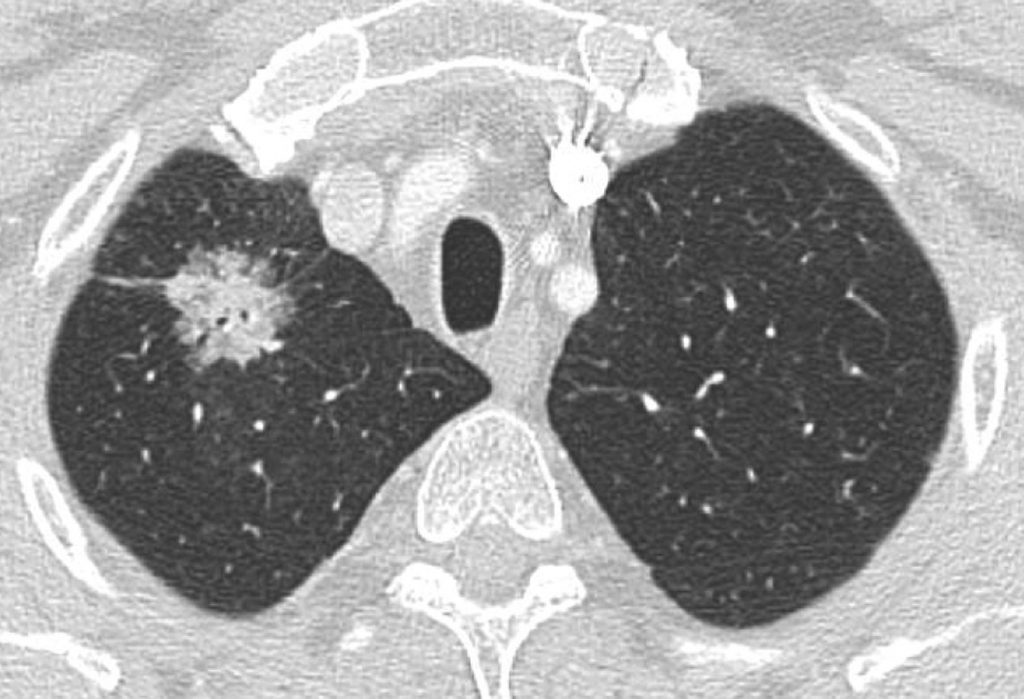

Fig. 101.2. Scanner thoracique (même patient que celui de la figure 101.1).
Macronodule du segment apical du lobe supérieur droit, de densité mixte (solide et « verre dépoli »), aux contours à la fois spiculés et lobulés. Après exérèse chirurgicale, l’examen anatomopathologique a révélé qu’il s’agissait d’un adénocarcinome bronchique.
Source : CERF, CNEBMN, 2022.

Les nœuds lymphatiques hilaires et médiastinaux sont en général considérés comme envahis s’ils sont trop volumineux (plus de 15 mm de petit axe) et/ou hypermétaboliques à la TEP-TDM au 18FDG (figure 101.3).
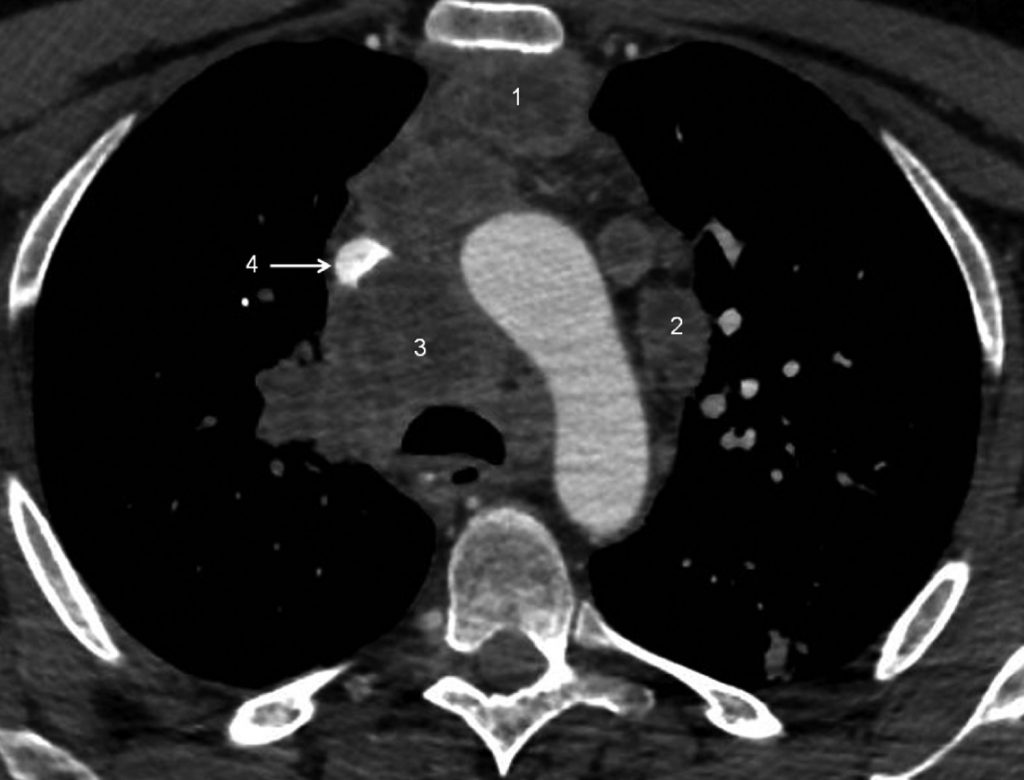

Fig. 101.3. Scanner thoracique.
Multiples adénomégalies médiastinales partiellement nécrotiques intéressant la loge thymique (1), la chaîne para-aortique (2) et la chaîne paratrachéale droite, ou loge de Barety (3). Sur cette coupe, la veine cave supérieure (4) apparaît partiellement laminée par les adénopathies mais reste perméable. Il s’agissait d’un carcinome à petites cellules.
Source : CERF, CNEBMN, 2022.
La TEP-TDM au 18FDG possède de meilleures sensibilité et spécificité que le scanner pour prédire l’envahissement lymphatique (figure 101.4).
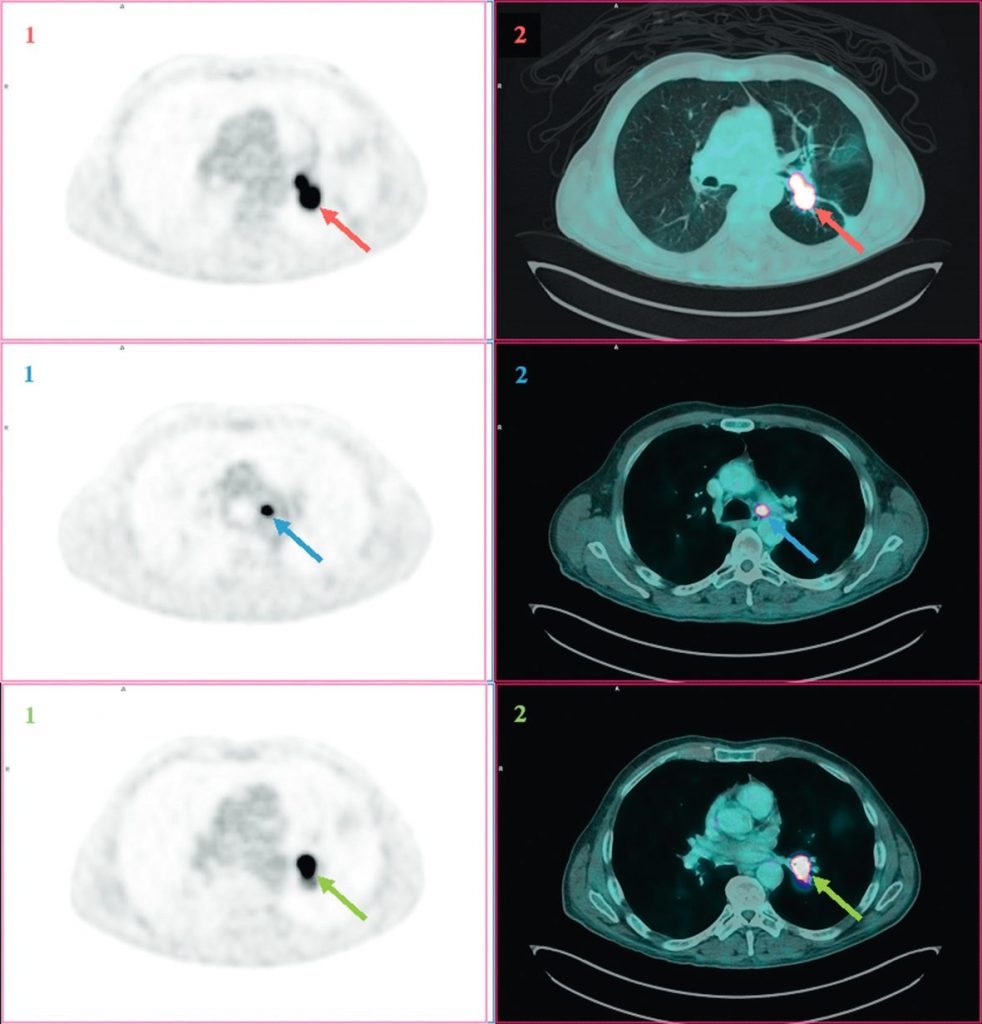

Fig. 101.4. Images TEP au 18FDG (1) et TEP au 18FDG fusionnée à la TDM (2) en coupes axiales.
Réalisées dans le cadre du bilan d’extension d’un carcinome bronchopulmonaire non à petites cellules lobaire inférieur gauche (flèche rouge).
Hyperfixation pathologique en regard d’adénopathie hilaire homolatérale (flèche verte) et de la fenêtre aortopulmonaire (flèche bleue).
Source : CERF, CNEBMN, 2022.

Les adénopathies trop nombreuses ou controlatérales à la tumeur bronchique (N3) sont des contre-indications à la chirurgie, de même que les localisations métastatiques à distance (le plus souvent osseuses, cérébrales, pleurales, pulmonaires ou surrénaliennes).
Tumeurs secondaires du poumon
I. Généralités

Le poumon constitue un filtre obligatoire pour l’ensemble de la masse sanguine et est, de ce fait, l’organe le plus fréquemment touché par les localisations tumorales à distance. Les cellules malignes peuvent migrer vers le poumon via le système sanguin ou le système lymphatique. Quel que soit le mode de dissémination, le pronostic des tumeurs pulmonaires secondaires est généralement péjoratif. Certaines métastases uniques pourront cependant être réséquées.

La dissémination des cellules tumorales est le plus souvent hématogène et concerne potentiellement tous les cancers (nodules pulmonaires ronds, multiples). La dissémination par voie lymphatique (lymphangite carcinomateuse) est plus rare et se rencontre essentiellement au cours des cancers bronchique, colorectal, mammaire ou génito-urinaire.
II. Stratégie d’exploration en imagerie
Le scanner du thorax est systématique dans le bilan d’extension et de surveillance de la plupart des néoplasies. La TEP-TDM au 18FDG est indiquée à la recherche d’un cancer primitif lorsque celui-ci est inconnu, ou à la recherche de localisations extrapulmonaires.

En cas de métastases pulmonaires prévalentes sans cancer primitif évident au scanner, une mammographie chez les femmes et un dosage du PSA chez les hommes seront également réalisés.
V. Sémiologie
A. Radiographie thoracique

Les métastases pulmonaires sont en général des images nodulaires multiples et bilatérales, arrondies, à contours nets (figures 101.5 et 101.6).
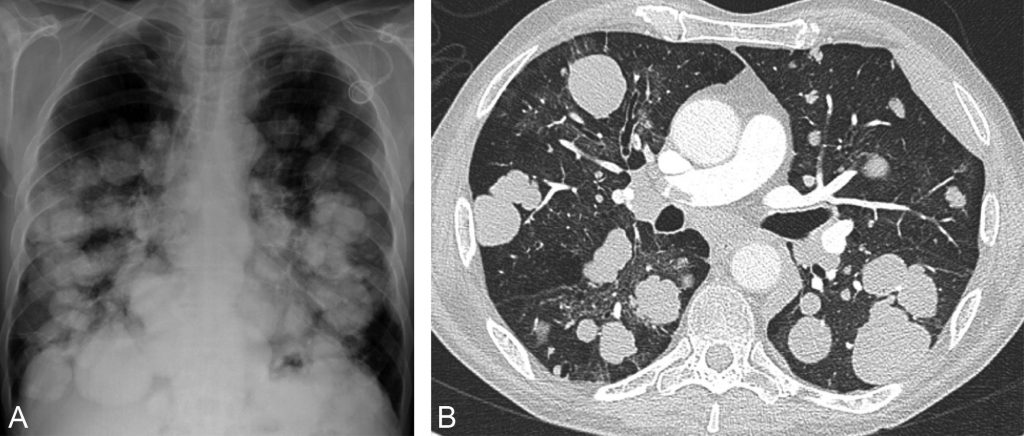
Fig. 101.5. Radiographie thoracique de face (A) et scanner thoracique (B).
Multiples macronodules réalisant une image en « lâcher de ballons ». Il s’agissait de métastases d’un carcinome bronchique non à petites cellules indifférencié. À noter sur la coupe scanographique l’existence d’une embolie dans l’artère pulmonaire droite.
Source : CERF, CNEBMN, 2022.
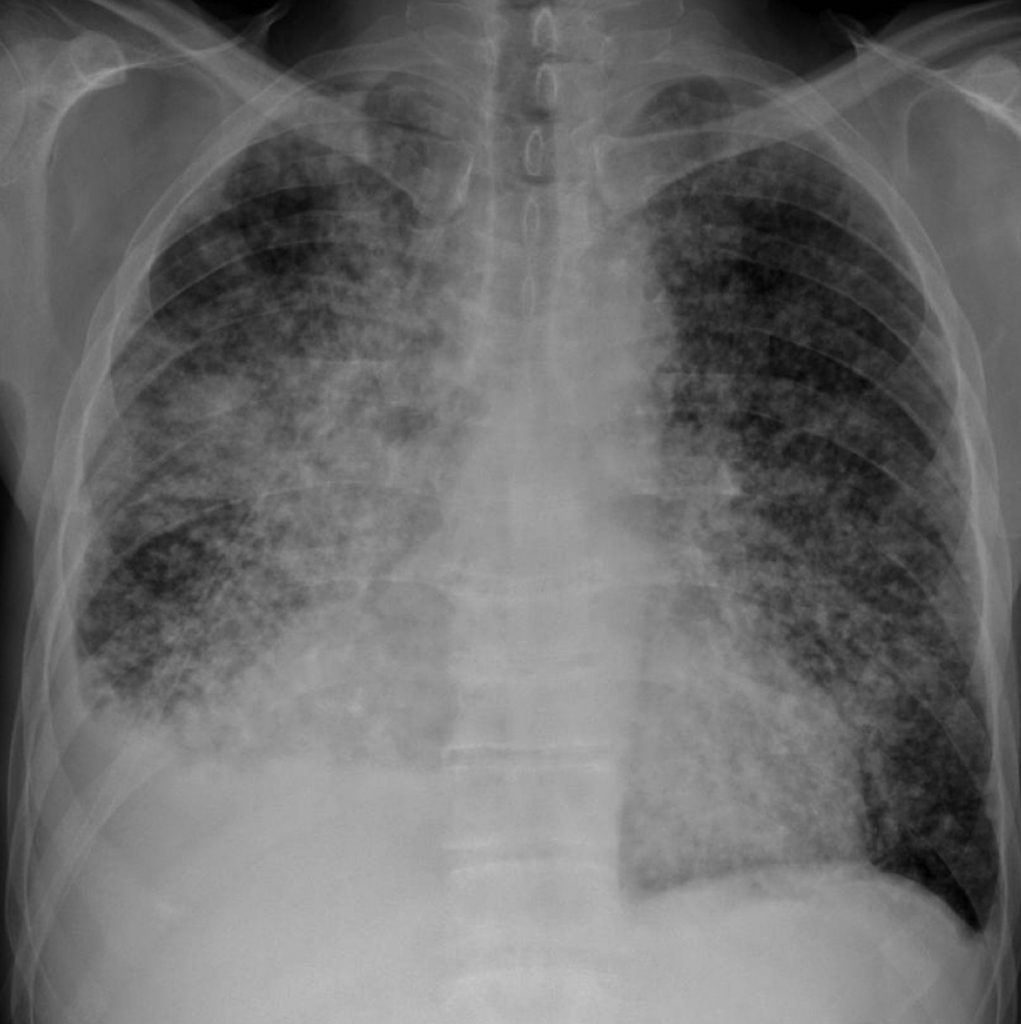
Fig. 101.6. Radiographie thoracique.
Syndrome micronodulaire bilatéral diffus associé à un épanchement pleural droit. Miliaire carcinomateuse sur néoplasie bronchique du lobe inférieur droit.
Source : CERF, CNEBMN, 2022.

La lymphangite se manifeste sous la forme d’un syndrome interstitiel (opacités réticulo-nodulaires) associé à un épaississement péribronchique, unilatéral le plus souvent ou bilatéral dans les formes très évoluées.
B. Tomodensitométrie

La taille des métastases pulmonaires est variable, depuis la miliaire carcinomateuse (multiples petites lésions millimétriques) jusqu’au « lâcher de ballons » (macronodules ou masses pulmonaires pouvant parfois s’excaver). L’intérêt principal du scanner est de permettre des mesures précises pour l’évaluation de la réponse thérapeutique. Si le primitif n’est pas connu, le scanner peut aussi guider une ponction-biopsie à visée diagnostique.

La lymphangite carcinomateuse associe un épaississement des parois bronchiques, des lignes septales irrégulières (correspondant à la dilatation des vaisseaux lymphatiques) et une micronodulation de distribution périlymphatique (figure 101.7).
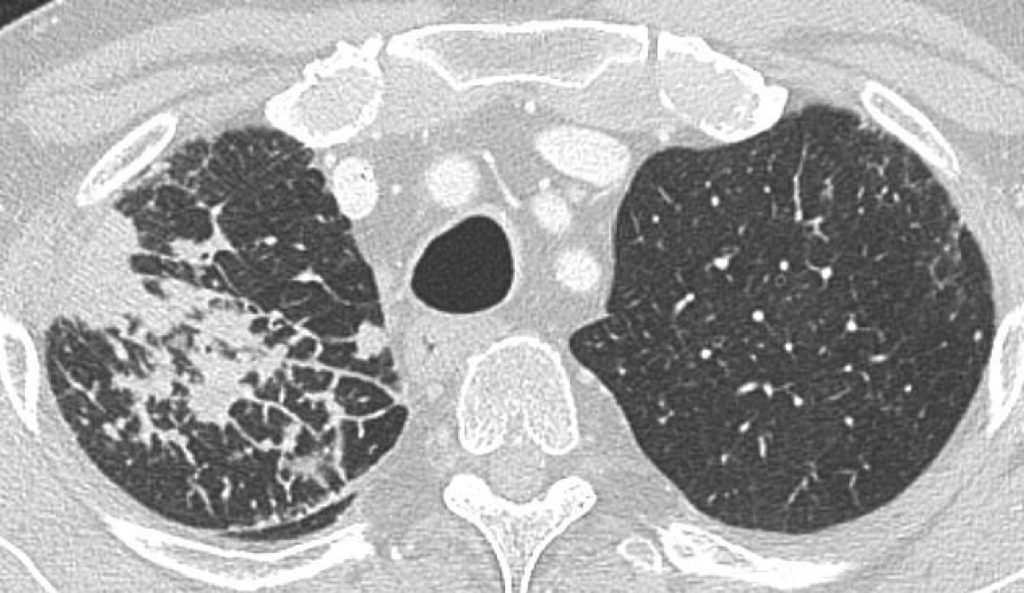
Fig. 101.7. Scanner thoracique.
L’apex pulmonaire droit est le siège de lignes septales associées à des nodules de taille variable de topographie sous-pleurale et périlymphatique. Il s’agissait d’une lymphangite carcinomateuse compliquant un adénocarcinome bronchique multifocal du poumon droit.
Source : CERF, CNEBMN, 2022.
C. TEP-TDM au 18FDG
La mise en évidence d’hyperfixations à la TEP-TDM au 18FDG confirmera l’atteinte tumorale. Elle orientera vers une localisation primitive par la mise en évidence d’une hyperfixation pathologique viscérale à distance.
Points clés
- Dans les tumeurs primitives, un scanner thoraco-abdominal-pelvien et encéphalique doit être réalisé pour caractériser la tumeur, guider les biopsies et établir le c-TNM fondé sur l’extension locorégionale, lymphatique et métastatique.
- Le scanner du thorax est systématique dans le bilan d’extension de la plupart des néoplasies. Il est plus performant que la radiographie si les lésions sont petites et/ou peu nombreuses, ainsi que dans la lymphangite carcinomateuse.
- La TEP-TDM au 18FDG est recommandée pour caractériser les nodules pulmonaires solides de taille supérieure à ou égale à 8 mm.
- La TEP-TDM au 18FDG est indiquée pour le bilan d’extension initial ganglionnaire et à distance des tumeurs pulmonaires.
- La TEP-TDM au 18FDG peut être proposée pour la recherche d’une tumeur primitive après la découverte de métastases pulmonaires sans primitif évident.