Plan de chapitre
ITEM 225 – Artériopathie oblitérante de l’aorte, des artères viscérales et des membres
inférieurs ; anévrismes
ITEM 238 – Souffle cardiaque chez l’enfant
ITEM 230 – Douleur thoracique aiguë et chronique
ITEM 332 – État de choc. Principales étiologies : (…) cardiogénique
ITEM 334 – Prise en charge immédiate préhospitalière et à l’arrivée à l’hôpital, évaluation des complications chez (…) un traumatisé thoracique
Diagnostic en imagerie d’une coarctation aortique
I. Généralités
II. Stratégie d’exploration en imagerie
– A. Diagnostic
– B. Suivi post-thérapeutique
III. Sémiologie
Diagnostic, bilan préthérapeutique et traitement endovasculaire d’un anévrisme de l’aorte abdominale
I. Généralités
II. Stratégie d’exploration en imagerie
– A. Diagnostic
– B. Suivi
– C. Radiologie interventionnelle
III. Sémiologie
Diagnostic d’un anévrisme de l’aorte abdominale rompu
I. Généralités
II. Stratégie d’exploration en imagerie
III. Sémiologie
Diagnostic, bilan préthérapeutique et traitement endovasculaire d’un anévrisme de l’aorte thoracique
I. Généralités
II. Stratégie d’exploration en imagerie
– A. Diagnostic
– B. Suivi
– C. Radiologie interventionnelle
III. Sémiologie
Dissections aortiques de types A et B : diagnostic en imagerie et traitement
endoluminal
I. Généralités
II. Stratégie d’exploration en imagerie
– A. Diagnostic
– B. Suivi
– C. Radiologie interventionnelle
III. Sémiologie
Rupture de l’isthme aortique
I. Généralités
II. Stratégie d’exploration en imagerie
– A. Diagnostic
– B. Radiologie interventionnelle
III. Sémiologie
Situations de départ
- 4 Douleur abdominale.
- 8 Masse abdominale.
- 161 Douleur thoracique.
- 178 Demande/prescription raisonnée et choix d’un examen diagnostique.
- 224 Découverte d’une anomalie abdominale à l’examen d’imagerie médicale.
- 233 Identifier/reconnaître les différents examens d’imagerie (type, fenêtre, séquences, incidences, injection).
Items, hiérarchisation des connaissances
ITEM 225 – Artériopathie oblitérante de l’aorte, des artères viscérales et des membres inférieurs ; anévrismes
| Rang | Rubrique | Intitulé |
| Définition | Définitions et fréquence de l’artériopathie oblitérante des membres inférieurs* | |
| Élements physiopathologiques | Connaître l’étiologie et les facteurs de risque de l’AOMI* | |
| Diagnostic positif | Connaître les manifestations cliniques et la classification de l’AOMI et savoir évoquer les diagnostics différentiels* | |
| Examens complémentaires | Savoir prescrire les examens complémentaires de première intention* | |
| Prise en charge | Connaître le traitement médical : traitement médicamenteux et principes du traitement chirurgical* | |
| Suivi et/ou pronostic | Connaître les complications et le pronostic : ischémie aiguë des membres inférieurs, morbimortalité cardiovasculaire* | |
| Diagnostic positif | Savoir définir et identifier les manifestations cliniques d’ischémie aiguë complète ou incomplète* | |
| Étiologie | Connaître les autres causes de l’ischémie aiguë* | |
| Identifier une urgence | Connaître les principes d’un traitement en urgence* | |
| Définition | Connaître la définition et l’histoire naturelle d’un anévrisme de l’aorte abdominale et savoir rechercher d’autres localisations anévrismales | |
| Étiologie | Connaître les principales étiologies des anévrismes de l’aorte abdominale et les principes du dépistage | |
| Diagnostic positif | Connaître les signes cliniques des anévrismes de l’aorte | |
| Examens complémentaires | Savoir comment faire le diagnostic des anévrysmes de l’aorte abdominale | |
| Prise en charge | Connaître les principes thérapeutiques d’un anévrisme de l’aorte abdominale | |
| Identifier une urgence | Savoir reconnaître et prendre en charge une situation d’urgence chez les patient porteur d’un anévrisme de l’aorte abdominale | |
| Définition | Définition de l’ischémie intestinale aiguë et chronique* | |
| Diagnostic positif | Connaître la sémiologie de l’ischémie intestinale aiguë et chronique : signes fonctionnels et signes physiques* |
ITEM 238 – Souffle cardiaque chez l’enfant
| Rang | Rubrique | Intitulé | Descriptif |
| Diagnostic positif | Sémiologie cardiovasculaire chez l’enfant | ||
| Définition | Définition d’un souffle cardiaque organique et non organique | Fréquence en fonction de l’âge | |
| Examens complémentaires | Connaître les apports des examens de première intention devant un souffle de l’enfant | Radiographie thoracique, ECG, échocardiographie | |
| Étiologie | Orientation étiologique des souffles cardiaques* | ||
ITEM 230 – Douleur thoracique aiguë et chronique
| Rang | Rubrique | Intitulé | Descriptif |
| Définition | Savoir définir une douleur thoracique aiguë* | ||
| Identifier une urgence | Savoir rechercher une détresse vitale devant une douleur thoracique* | Détresse respiratoire ou hémodynamique, troubles de la conscience | |
| Identifier une urgence | Identifier les signes de gravité imposant des décisions thérapeutiques immédiates* | ||
| Diagnostic positif | Savoir évoquer les 4 urgences cardio-vasculaires devant une douleur thoracique* | Dissection aortique, syndromes coronariens aigus, péricardite avec tamponnade, embolie pulmonaire | |
| Diagnostic positif | Connaître la sémiologie clinique fonctionnelle et physique de le dissection aortique* | Redondant avec item 226, 234, 235 | |
| Diagnostic positif | Connaître la démarche diagnostique des 4 urgences cardio-vasculaires* | Terrain évocateur, caractéristiques de la douleur thoracique, particularités de l’examen clinique | |
| Examens complémentaires | Connaître les anomalies électrocardiographiques des 4 urgences cardio-vasculaires* | ||
| Examens complémentaires | Connaître la place et les anomalies de la radiographie thoracique des 4 urgences cardio-vasculaires | ||
| Examens complémentaires | Connaître les examens biologiques à prescrire et leur interprétation des 4 urgences cardio-vasculaires* | ||
| Examens complémentaires | Connaître la place de la coronarographie dans le diagnostic et les principes de prise en charge du syndrome coronarien aigu* | ||
| Examens complémentaires | Connaître la place de l’échocardiographie, de l’ETO et du scanner thoracique dans le diagnostic de dissection aortique | ||
| Étiologie | Devant un angor d’effort, connaître les principales causes d’angor fonctionnel* | Rétrécissement aortique serré, cardiomyopathie hypertrophique ,tachycardies (fibrillation atriale), anémie, hyperthyroïdie | |
| Étiologie | Connaître les principales causes thoraciques de douleur aiguë en dehors des quatre urgences cardiovasculaires* | Pneumonie, pneumothorax. Renvoyer aux items correspondants | |
| Étiologie | Connaître les principales causes extra-thoraciques de douleur thoracique* | Pancréatite, cholécystite, ulcère, RGO. Renvoyer aux items correspondants | |
ITEM 332 – État de choc. Principales étiologies : (…) cardiogénique
| Rang | Rubrique | Intitulé | Descriptif |
| Définition | Connaître la définition de l’état de choc* | Savoir définir un état de choc | |
| Étiologies | Connaître les principales étiologies des états de choc* | Cardiogénique, obstructif, septique, hémorragique et anaphylactique | |
| Éléments physiopathologiques | Connaître la physiopathologie des états de choc, selon leur étiologie* | Connaître les principaux mécanismes hémodynamiques, inflammatoires et métaboliques conduisant aux défaillances d’organes | |
| Diagnostic positif | Connaître les signes cliniques d’un état de choc* | Reconnaître l’hypotension artérielle et savoir rechercher les signes de défaillance d’organes, savoir rechercher une hyperlactatémie | |
| Diagnostic positif | Connaître les éléments d’anamnèse et cliniques pour le diagnostic étiologique selon l’anamnèse et la clinique* | Savoir recueillir les éléments anamnestiques et cliniques nécessaires à l’orientation diagnostique | |
| Examens complémentaires | Savoir caractériser le type d’état de choc | Savoir recourir aux examens complémentaires permettant de caractériser l’étiologie de l’état de choc (échocardiographie, tomodensitométrie, biologie) | |
| Examens complémentaires | Connaître la stratégie d’exploration devant un choc hémorragique* | ||
| Prise en charge | Connaître les éléments de prise en charge immédiate d’un état de choc* | Arrêt du mécanisme causal (hémorragie, anaphylaxie), oxygénation, remplissage vasculaire adapté, appel à l’aide | |
| Prise en charge | Connaître les principes de prise en charge du choc hémorragique* | Stratégie transfusionnelle ; Connaître les principes d’hémostase (médicamenteux, chirurgie, radiologie interventionnelle de l’artère causale d’un choc hemorragique, endoscopie…) | |
| Prise en charge | Connaître les principes de prise en charge du choc septique* | ||
| Prise en charge | Connaître les principes de prise en charge du choc cardiogénique* | ||
| Prise en charge | Connaître les principes de prise en charge du choc obstructif* | ||
| Prise en charge | Connaître les principes de prise en charge du choc anaphylactique* | ||
ITEM 334 – Prise en charge immédiate préhospitalière et à l’arrivée à l’hôpital, évaluation des complications chez (…) un traumatisé thoracique
| Rang | Rubrique | Intitulé | Descriptif |
| Éléments physiopathologiques | Connaître la physiopathologie de l’atteinte des organes intrathoraciques après traumatisme | Décrire les mécanismes d’atteinte des organes intrathoraciques et l’incidence des atteintes | |
| Diagnostic positif | Savoir suspecter un traumatisme thoracique* | Identifier les signes évocateurs : anamnèse, inspection (signe de la ceinture, contusion, plaie) | |
| Examens complémentaires | Savoir demander les examens complémentaires permettant le diagnostic de traumatisme thoracique | Échographie pleuropulmonaire, tomodensitométrie thoraco-abdominale avec injection de produit de contraste, radiographie de thorax, électrocardiogramme | |
| Examens complémentaires | Savoir reconnaître un hémothorax et un pneumothorax sur une radiographie | ||
| Contenu multimédia | Radiographies d’hémothorax et de pneumothorax | ||
| Identifier une urgence | Savoir identifier les situations indiquant le recours à une thérapeutique de sauvetage* | Pneumothorax suffoquant, syndrome hémorragique, détresse respiratoire, choc | |
| Prise en charge | Connaître les principes de la prise en charge d’un traumatisme thoracique* | Analgésie multimodale, drainage thoracique, assistance ventilatoire non invasive, exploration chirurgicale des traumatismes pénétrants, avis chirurgical spécialisé pour les cas complexes (rupture de l’isthme aortique, volet thoracique, lésions diaphragmatiques et cardiaques) | |
Diagnostic en imagerie d’une coarctation aortique
I. Généralités

La coarctation de l’aorte est un rétrécissement de l’aorte descendante associé à une circulation collatérale de dérivation. Cette malformation congénitale se révèle chez l’adulte jeune ou chez l’enfant, voire en anténatal, surtout quand elle est associée à d’autres malformations, notamment cardiaques (bicuspidie aortique par exemple) ou à un syndrome de Turner.
Habituellement asymptomatique, la coarctation doit être recherchée en palpant systématiquement les pouls fémoraux, justifiant une échographie postnatale ou, plus tard, sur une radiographie thoracique devant la présence d’empreintes costales, de pouls fémoraux diminués, d’une hypertension artérielle, d’un souffle ou d’une asymétrie tensionnelle bras-jambes.
Actuellement, les coarctations natives bénéficient de plus en plus d’un traitement endovasculaire premier plutôt qu’un traitement chirurgical. Les re-coarctations opérées sont traitées par des angioplasties.
II. Stratégie d’exploration en imagerie
A. Diagnostic
Chez le nouveau-né et le nourrisson, l’échographie cardiaque transthoracique est suffisante pour affirmer le diagnostic. Elle apprécie également le retentissement et les anomalies cardiaques associées.
L’angio-IRM — plutôt que l’angioscanner pour éviter l’exposition aux rayons X chez l’enfant jeune, conformément à la directive Euratom 97/43 — permet de mettre en évidence la sténose aortique et de faire le bilan complet de l’affection en préthérapeutique : recherche d’hypoplasie de l’arc aortique, quantification et longueur de la sténose et topographie exacte, étude de la valve aortique et de la fonction cardiaque (figure 36.1).
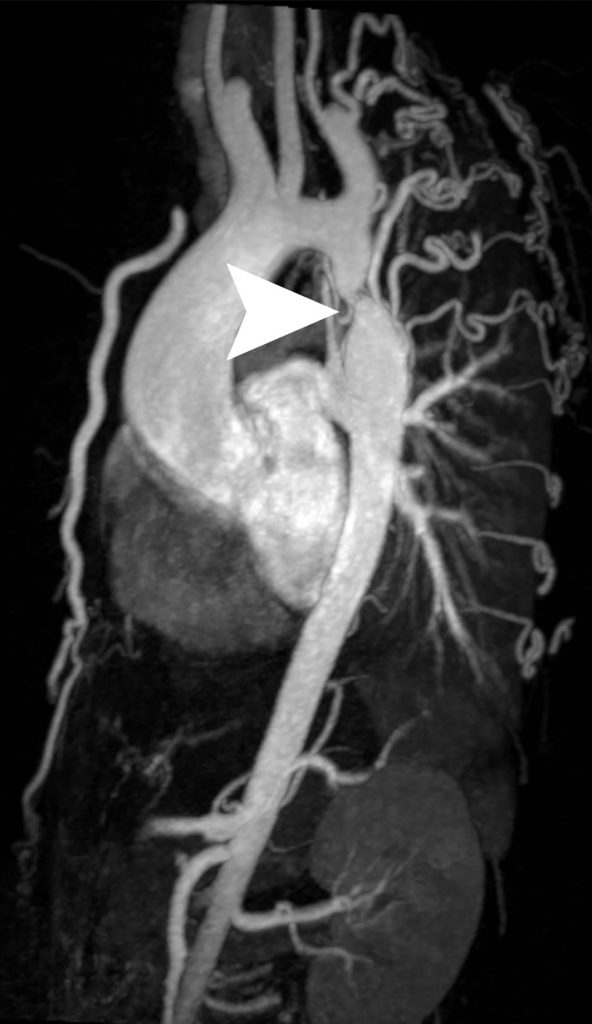
Fig. 36.1. Angio-IRM de l’ensemble de l’aorte en reconstruction 3D et vue sagittale oblique.
Coarctation de l’aorte : sténose aortique courte en regard de l’isthme (tête de flèche), avec dilatation post-sténotique et de nombreuses artères collatérales hypertrophiées (notamment les artères intercostales).
Source : CERF, CNEBMN, 2022.
Le cathétérisme aortique permet de mesurer le gradient de pression, pour planifier l’intervention.
B. Suivi post-thérapeutique
Il est assuré par échographie-doppler et angio-IRM, permettant de détecter d’éventuelles récidives ou anévrismes au niveau du pontage et de surveiller l’état cardiaque.
III. Sémiologie
La coarctation aortique se présente le plus souvent sous la forme d’une sténose courte de l’aorte thoracique, siégeant en regard de l’isthme, avec parfois une dilatation post-sténotique de l’aorte sous-jacente et une dilatation des artères intercostales.
Points clés
- Diagnostic et bilan préthérapeutique par échocardiographie et angio-IRM.
- Suivi par écho-doppler et angio-IRM aortique.
Diagnostic, bilan préthérapeutique et traitement endovasculaire d’un anévrisme de l’aorte abdominale
I. Généralités
L’anévrisme de l’aorte abdominale est une dilatation localisée de plus de 50 % du calibre de l’aorte abdominale avec perte du parallélisme de ses bords. La découverte peut être fortuite lors d’une échographie abdominale de dépistage, un scanner ou lors de l’examen clinique devant une masse battante, pulsatile et expansive. L’évolution se fait vers la rupture.
La surveillance de tout anévrisme diagnostiqué est indispensable.
Une croissance rapide (plus de 5 mm en 6 mois) ou un diamètre total de plus de 50 mm sont des indications opératoires formelles.
En cas d’anévrisme de l’aorte, il est indispensable de rechercher d’autres anévrismes iliaques, fémoraux et poplités, associés dans 25 % des cas, et de faire la recherche d’autres localisations athéromateuses (coronaires, carotides, collatérales aortiques et artères des membres inférieurs).
II. Stratégie d’exploration en imagerie
A. Diagnostic
1. Échographie abdominale
L’échographie abdominale est l’examen de première intention qui permet de dépister un anévrisme de l’aorte abdominale ou de confirmer une suspicion clinique. Elle est proposée dans les campagnes de dépistage pour des populations ciblées.
Si ce diagnostic est facile, la mensuration exacte de l’aorte (le plus grand diamètre externe mesuré perpendiculairement à l’axe du vaisseau) doit répondre à des critères techniques très précis (figure 36.2A).
En revanche, cet examen ne permet pas de faire le bilan lésionnel complet, indispensable à une prise en charge thérapeutique.
2. Angioscanner
Cet examen permet de confirmer le diagnostic si nécessaire et surtout d’en préciser les caractéristiques morphologiques et topographiques.
Toute suspicion d’anévrisme de l’aorte abdominale doit être explorée par un angioscanner abdominal.
Il permet de préciser sa taille, sa forme (fusiforme ou sacciforme), sa topographie par rapport aux artères rénales et à la bifurcation aortique, son extension aux branches collatérales de l’aorte, la présence d’anomalies pariétales (calcifications, inflammation péri-anévrismale), les sténoses des collatérales viscérales, iliaques, etc. (figure 36.2B et 36.3A).
En cas de douleur abdominale ou lombaire chez un patient connu porteur d’un anévrisme de l’aorte, le scanner doit être réalisé en urgence à la recherche d’une fissuration (voir plus loin « Diagnostic d’un anévrisme de l’aorte abdominale rompu »).
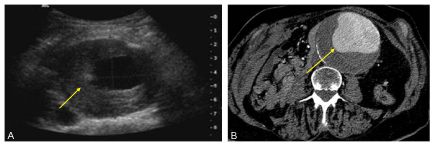
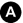
Fig. 36.2. Anévrisme de l’aorte abdominale.
En échographie (A) et en scanner (B), l’aorte apparaît très dilatée avec ici présence de thrombus mural (flèches).
Source : CERF, CNEBMN, 2022.
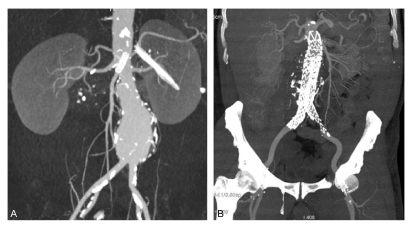
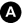
Fig. 36.3. Anévrisme de l’aorte abdominale.
Les reconstructions TDM frontales (A) montrent la topographie du sac anévrismal par rapport aux artères rénales et à la bifurcation aortique : il s’agit ici d’un anévrisme sous-rénal. Après traitement par mise en place d’une endoprothèse couverte, le scanner en reconstruction frontale montre la prothèse dans la lumière aortique avec son armature de crochets métalliques et la thrombose du sac anévrismal autour (B).
Source : CERF, CNEBMN, 2022.
3. Angio-IRM
L’angio-IRM peut également être utilisée pour le bilan préthérapeutique ou pour la surveillance s’il existe des contre-indications à la réalisation de l’angioscanner, mais l’étude des parois est de moins bonne qualité (calcifications moins bien visibles et moins bonne résolution spatiale qu’en scanner).
B. Suivi
La surveillance d’un anévrisme non opéré doit être régulière : c’est l’évolution du plus grand diamètre externe qui permet d’apprécier son évolutivité. Elle peut être faite en échographie, à condition d’utiliser une technique reproductible, ou par angioscanner.
C. Radiologie interventionnelle
Quand le risque opératoire est élevé et que la morphologie de l’aorte et de l’anévrisme s’y prête, le traitement endovasculaire par mise en place d’une endoprothèse métallique couverte appelée stent-graft est possible. La prothèse, qui est déployée par un cathéter introduit par voie fémorale, se déploie dans l’aorte en regard, au-dessus et au-dessous du sac anévrismal, réalisant un conduit étanche et rigide qui exclut l’anévrisme de la circulation (figure 36.3B).
III. Sémiologie
Un anévrisme de l’aorte se présente sous la forme d’une ectasie de la lumière aortique, associée le plus souvent à un thrombus pariétal. En scanner, on perçoit facilement que le diamètre de l’aorte dépasse celui du corps vertébral (cf. figure 36.2B) :
- la lumière aortique circulante apparaît anéchogène en échographie et se rehausse en scanner après injection ;
- le thrombus pariétal apparaît échogène en échographie et ne se rehausse pas en scanner après injection (cf. figure 36.2, A et B).
Points clés
- La détection repose sur la mise en évidence d’un diamètre aortique externe augmenté de plus de 50 % du diamètre de l’aorte abdominale normale, en échographie ou en scanner.
- Le diagnostic, le bilan préthérapeutique et la surveillance des anévrismes de l’aorte abdominale se font par angioscanner.
- L’angio-IRM peut également être utilisée pour la surveillance.
- Le traitement par voie endovasculaire des anévrismes de l’aorte est possible.
Diagnostic d’un anévrisme de l’aorte abdominale rompu
I. Généralités
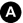
L’évolution des anévrismes de l’aorte abdominale se fait vers la rupture, parfois annoncée par l’apparition de douleurs abdominales ou lombaires, mais plus souvent révélée par un choc hémorragique qui, dans la plupart des cas, entraîne le décès du patient avant son arrivée à l’hôpital.
Jusqu’à preuve du contraire, toute douleur abdominale ou lombaire violente chez un sujet porteur d’un anévrisme de l’aorte abdominale est suspecte d’être une rupture aortique et doit entraîner une prise en charge adaptée et rapide pour traitement urgent.
Si le diagnostic est évoqué chez un patient hémodynamiquement instable, celui-ci doit alors être immédiatement et directement dirigé vers le bloc opératoire sans faire d’exploration qui pourrait entraîner une perte de temps.
II. Stratégie d’exploration en imagerie
L’exploration d’un anévrisme suspect de rupture ne doit pas retarder la prise en charge thérapeutique.
En cas de douleur lombaire aiguë chez un patient âgé, non connu porteur d’un anévrisme de l’aorte abdominale, il faut pratiquer une échographie abdominale à sa recherche (diagnostic différentiel de la colique néphrétique). En cas de positivité, un angioscanner doit être effectué en urgence, en l’absence de signes de choc.
En cas de douleur abdominale ou lombaire violente chez un sujet porteur d’un anévrisme de l’aorte abdominale, et en l’absence de signes de choc, un angioscanner doit être pratiqué d’emblée en urgence.
En cas de rupture, le scanner, même réalisé sans injection de produit de contraste, montre un épanchement liquidien hématique péri-aortique, le plus souvent rétropéritonéal.
L’angioscanner, en plus du diagnostic de rupture rétropéritonéale, permet, le cas échéant, le diagnostic de rupture dans le tube digestif (responsable de méléna) ou dans la veine cave inférieure (responsable d’une fistule aorto-cave) et permet un bilan préthérapeutique plus précis, en particulier quand un traitement endovasculaire de l’anévrisme est envisagé en urgence.
III. Sémiologie
Le diagnostic repose, en scanner abdominal, sur la présence d’un anévrisme de l’aorte abdominale associé à un épanchement hématique péri-aortique (figure 36.4). Parfois, on met en évidence la zone de fissuration avec, très rarement, une extravasation de produit de contraste.
Points clés
- Urgence vitale à suspecter jusqu’à preuve du contraire devant l’association douleur abdominale et anévrisme de l’aorte abdominale connu et l’association douleur abdominale et collapsus hypovolémique et hémorragique.
- Scanner en extrême urgence, sans retarder la prise en charge thérapeutique, recherchant un épanchement péri-aortique.
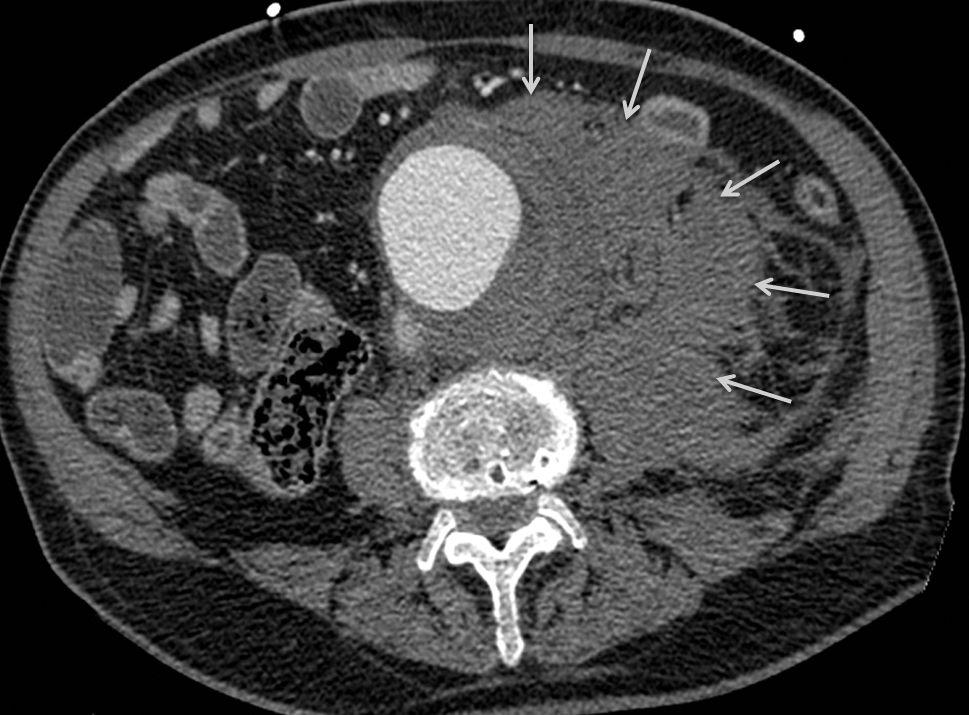
Fig. 36.4. Rupture d’un anévrisme de l’aorte abdominale se traduisant par la présence d’un volumineux hématome rétropéritonéal latéro-aortique gauche (flèches).
Source : CERF, CNEBMN, 2022.
Diagnostic, bilan préthérapeutique et traitement endovasculaire d’un anévrisme de l’aorte thoracique
I. Généralités
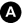
L’anévrisme de l’aorte thoracique est une dilatation localisée de plus de 50 % du calibre de l’aorte avec perte du parallélisme de ses bords. La découverte peut être fortuite lors d’une radiographie thoracique, un scanner thoracique ou une échographie cardiaque. L’évolution se fait vers la rupture parfois annoncée par l’apparition de douleurs thoraciques mais plus souvent révélée par un choc hémorragique qui, dans la plupart des cas, entraîne le décès du patient avant son arrivée à l’hôpital.
Jusqu’à preuve du contraire, toute douleur thoracique violente chez un sujet porteur d’un anévrisme de l’aorte thoracique est suspecte d’être une rupture aortique et doit entraîner une prise en charge urgente, le plus souvent par la mise en place d’une endoprothèse dans l’aorte thoracique si l’anévrisme est localisé dans l’aorte thoracique descendante.
L’anévrisme de l’aorte thoracique peut aussi être révélé par une embolie artérielle distale d’athérome ou des signes de compression d’organes de voisinage.
La surveillance de tout anévrisme diagnostiqué est indispensable, en sachant qu’une croissance rapide de plus de 5 mm en 6 mois ou un diamètre total supérieur à 60 mm sont des indications opératoires formelles.
II. Stratégie d’exploration en imagerie
A. Diagnostic
1. Angioscanner
Toute suspicion d’anévrisme de l’aorte thoracique doit être explorée par un angioscanner thoracique qui précise le volume, la topographie de l’anévrisme et son extension aux branches collatérales (troncs supra-aortiques), ainsi que la présence d’anomalies pariétales : thrombus, ulcérations, inflammation (figure 36.5).
En cas de douleur thoracique chez un sujet porteur d’anévrisme de l’aorte thoracique, un angioscanner doit être réalisé en urgence à la recherche d’une rupture aortique.
En cas de rupture aortique, l’angioscanner montrera un épanchement péri-aortique (médiastinal et/ou pleural) associé à l’anévrisme (figure 36.6).
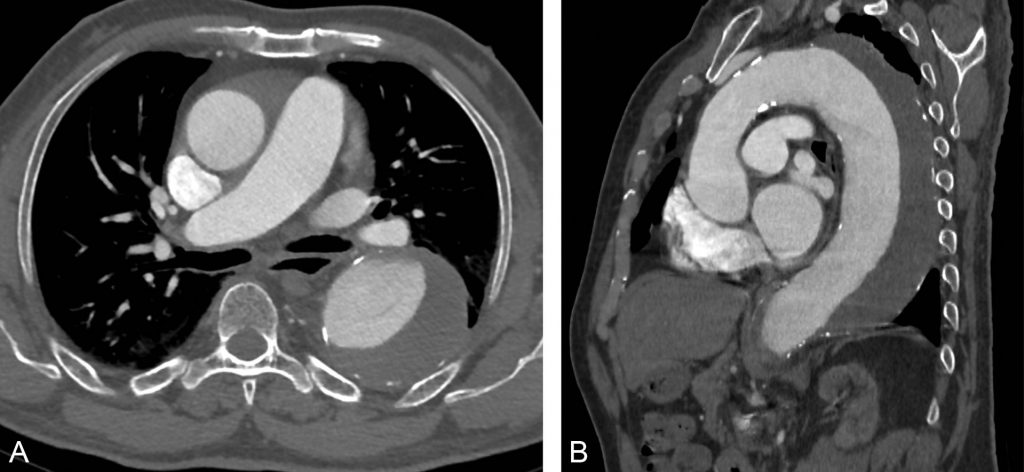
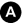
Fig. 36.5. Anévrisme de l’aorte thoracique en angioscanner.
Il se traduit sur la coupe axiale (A) par une augmentation du diamètre de l’aorte descendante qui dépasse celui de l’aorte ascendante. La reconstruction sagittale oblique montre que cet anévrisme est développé dans la concavité aortique au niveau de l’isthme, après l’origine de l’artère subclavière gauche (B).
Source : CERF, CNEBMN, 2022.
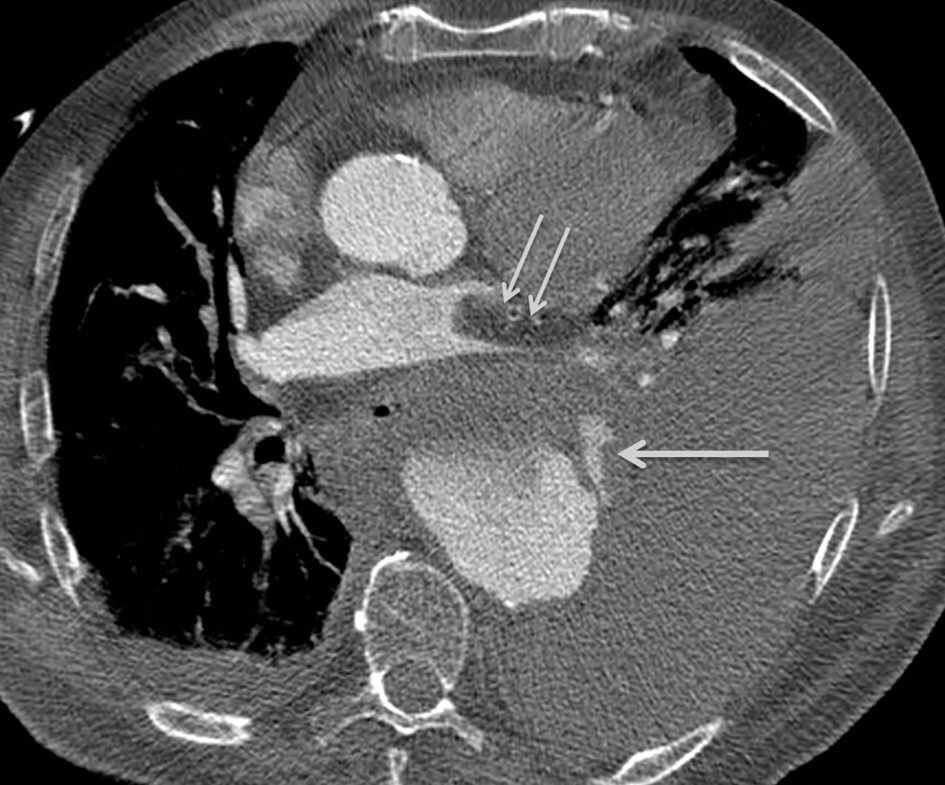
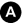
Fig. 36.6. Exemple de rupture d’anévrisme de l’aorte thoracique en angioscanner.
Celle-ci se traduit par la présence d’un hémomédiastin autour de l’aorte, d’un volumineux hémothorax gauche. La zone de fissuration est bien visible (flèche). À noter la présence concomitante d’une embolie pulmonaire dans l’artère pulmonaire gauche (double flèche).
Source : CERF, CNEBMN, 2022.
2. Angio-IRM
Elle peut se substituer à l’angioscanner, en dehors de l’urgence, en cas d’insuffisance rénale ou d’intolérance aux produits de contraste iodés.
3. Échographie
L’échographie transthoracique n’explore que le premier segment de l’aorte ascendante et ne permet pas l’étude de l’arc aortique ni celle de l’aorte thoracique descendante. En revanche, cette dernière peut être parfaitement visualisée en échographie transœsophagienne.
B. Suivi
L’angioscanner est l’examen qui permet la surveillance du plus grand diamètre de l’aorte anévrismale, mesuré perpendiculairement à l’axe du vaisseau, et de poser les indications thérapeutiques.
C. Radiologie interventionnelle
Le traitement chirurgical conventionnel est la règle pour l’aorte ascendante.
Le traitement endovasculaire est possible pour l’aorte descendante :
- il consiste à introduire par une artère périphérique, habituellement l’artère fémorale, jusque dans l’aorte thoracique et à déployer sur place une endoprothèse métallique couverte d’un tissu étanche appelée stent-graft, permettant ainsi d’exclure le sac anévrismal de la circulation aortique ;
- il doit être discuté en première intention dans les formes anatomiques favorables de l’aorte thoracique descendante car il a un taux de complications beaucoup plus faible que la chirurgie conventionnelle.
III. Sémiologie
Un anévrisme de l’aorte thoracique se présente sous la forme d’une ectasie de la lumière aortique, associée souvent à un thrombus pariétal (cf. figure 36.5A, B).
En scanner :
- ses parois sont souvent calcifiées ;
- après injection, la lumière aortique circulante se rehausse alors que le thrombus pariétal ne se rehausse pas ;
- le diamètre de l’aorte descendante dépasse celui de l’aorte ascendante.
Points clés
- Diagnostic et surveillance des anévrismes de l’aorte thoracique par angioscanner.
- Toute douleur thoracique chez un sujet porteur d’un anévrisme de l’aorte thoracique est une suspicion de rupture aortique et impose la réalisation d’un scanner en urgence si le patient est hémodynamiquement stable.
- Le traitement endovasculaire des anévrismes de l’aorte thoracique descendante est faisable et doit être réalisé en première intention en urgence si rupture.
Dissections aortiques de types A et B : diagnostic en imagerie et traitement endoluminal
I. Généralités
La dissection aortique est due à un clivage longitudinal de la paroi de l’aorte qui siège au niveau de la média. L’espace disséqué communique avec la lumière aortique par une ou plusieurs déchirures intimales appelées entrées ou réentrées. Selon la classification de Stanford :
- dans les dissections de type A, la dissection atteint l’aorte ascendante, c’est-à-dire entre l’anneau aortique et l’artère subclavière gauche ; l’évolution se fait rapidement vers la rupture intrapéricardique en l’absence de prise en charge urgente dans un service de chirurgie cardiovasculaire ;
- dans les dissections de type B, la dissection atteint l’aorte descendante, après l’origine de l’artère subclavière gauche.
Dans les deux cas, le faux chenal peut comprimer le vrai chenal circulant de l’aorte ou ses branches, et entraîner une malperfusion des organes en aval. Lorsque le faux chenal est thrombosé, il s’agit alors d’un hématome disséquant.
En cas de malperfusion ou de dissection de type B compliquée de rupture, un traitement endovasculaire peut être proposé.
II. Stratégie d’exploration en imagerie
A. Diagnostic
1. Angioscanner cervico-thoraco-abdomino-pelvien
L’angioscanner est l’examen clé du diagnostic positif, hautement sensible et spécifique.
Une acquisition sans injection de produit de contraste iodé est obligatoire pour faire le diagnostic d’hématome intrapariétal.
Il permet un bilan préthérapeutique précis de :
- l’extension aux collatérales aortiques ;
- l’extension à l’anneau aortique et aux artères coronaires.
De plus, il détecte les complications telles que :
- les hématomes péri-aortiques liés aux ruptures ;
- les défauts de rehaussement des organes malperfusés.
2. Échographie
L’échographie transthoracique peut montrer un hémopéricarde.
L’échographie transœsophagienne permet également le diagnostic positif de dissection de type A, mais ne permet pas l’étude de l’arc aortique et des troncs supra-aortiques, de l’aorte thoracique descendante, de l’aorte abdominale et des collatérales aortiques.
3. Radiographie thoracique
Elle peut mettre en évidence un élargissement du médiastin et un déplacement des calcifications du bouton aortique, c’est-à-dire de l’arc aortique, de topographie intimale vers le dedans.
B. Suivi
L’angioscanner permet de suivre l’évolution d’une dissection non traitée (type B) ou opérée (type A).
L’angio-IRM peut se substituer au précédent pour assurer cette surveillance de façon non irradiante.
Dans les types B, il faut surveiller tout particulièrement le calibre respectif du vrai chenal qui peut être comprimé, et du faux chenal qui peut subir une dilatation anévrismale.
C. Radiologie interventionnelle
Pour les dissections de type A opérées et B, compliquées de malperfusion, le traitement de l’ischémie digestive et rénale ou de l’ischémie des membres inférieurs repose sur les techniques endovasculaires : réouverture de la vraie lumière par mise en place de stent-grafts intra-aortiques, stenting des artères viscérales ou iliaques occluses, ou fenestration, selon les cas. Les anévrismes du faux chenal thoracique descendant peuvent être traités par endoprothèses.
III. Sémiologie
La dissection apparaît, en échographie ou sur les coupes tomodensitométriques transversales injectées et les reconstructions sagittales, sous la forme d’un flap intimal qui divise l’artère en deux chenaux :
- le vrai chenal, qui communique avec la lumière aortique depuis le ventricule gauche ;
- le faux chenal, qui prend naissance sur l’aorte ascendante ou horizontale dans le type A (figure 36.7) et après la naissance de l’artère subclavière gauche dans le type B (figure 36.8). Il peut circuler plus lentement, voire se thromboser (responsable d’un hématome pariétal), comprimer ou pas le vrai chenal, ou subir dans le temps une évolution anévrismale.
L’hématome pariétal apparaît sous la forme d’une paroi épaissie hyperdense spontanément sur les coupes tomodensitométriques sans injection.
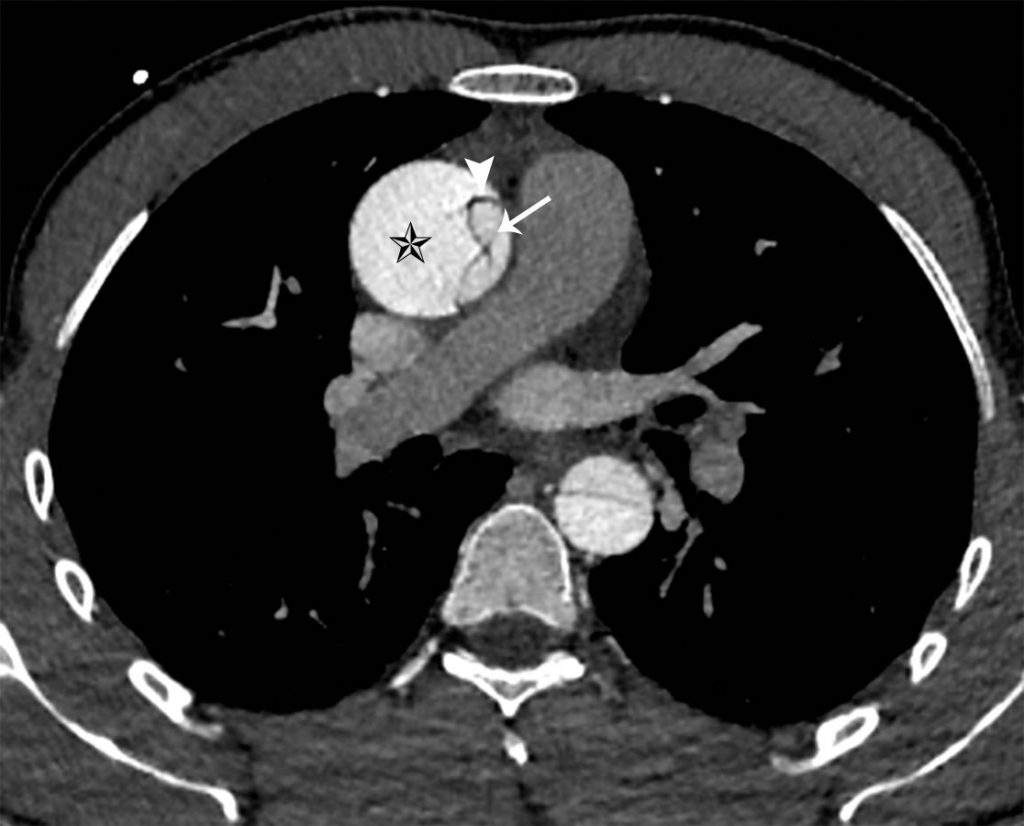
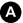
Fig. 36.7. Angioscanner thoracique en coupe axiale d’un anévrisme de l’aorte ascendante associée à une dissection de type A avec un flap intimal (tête de flèche) dans l’aorte ascendante et dans l’aorte descendante, séparant le vrai (flèche) et le faux chenal (étoile).
Source : CERF, CNEBMN, 2022.
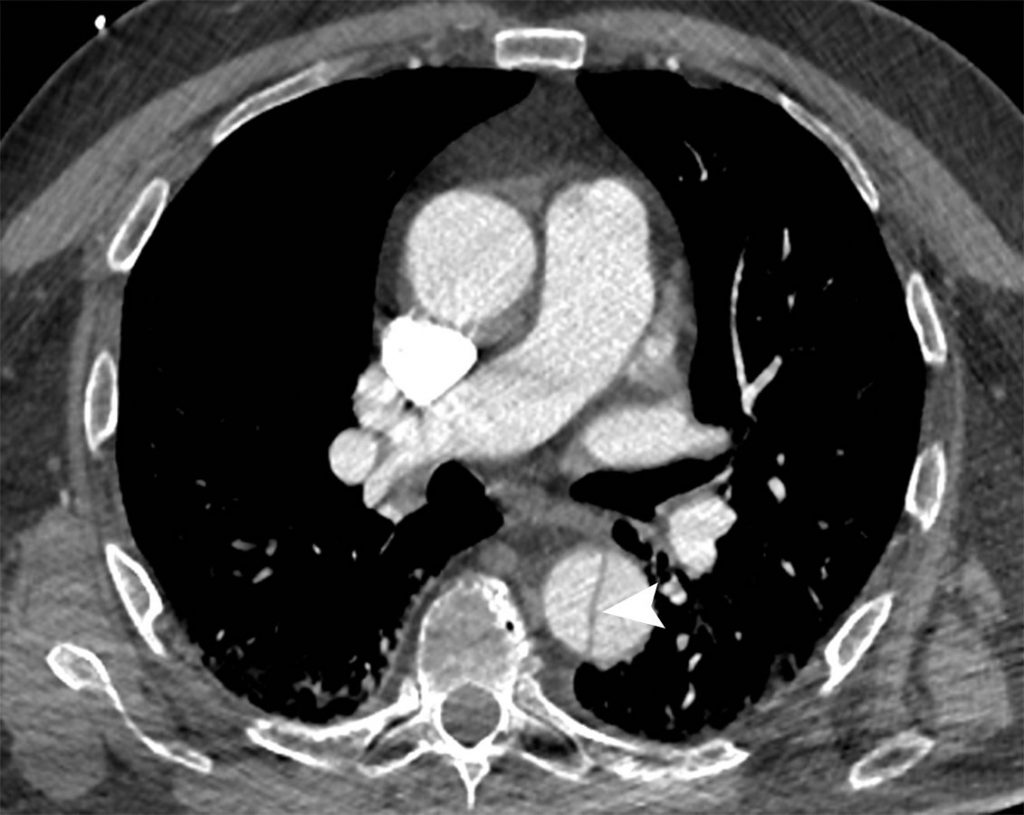
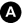
Fig. 36.8. Angioscanner thoracique en coupe axiale d’une dissection de type B avec un flap intimal (tête de flèche) dans l’aorte descendante.
Source : CERF, CNEBMN, 2022.
Points clés
- L’angioscanner thoraco-abdomino-pelvien est l’examen clé pour le diagnostic et l’extension de la dissection avec mise en évidence d’un flap intimal séparant le vrai chenal du faux chenal.
- Il permet la recherche des complications : rupture aortique (figure 36.9) avec épanchement hématique médiastinal et/ou pleural, malperfusion des organes par extension aux artères collatérales ou par compression du vrai chenal par le faux chenal (figure 36.10), et évolution anévrismale.
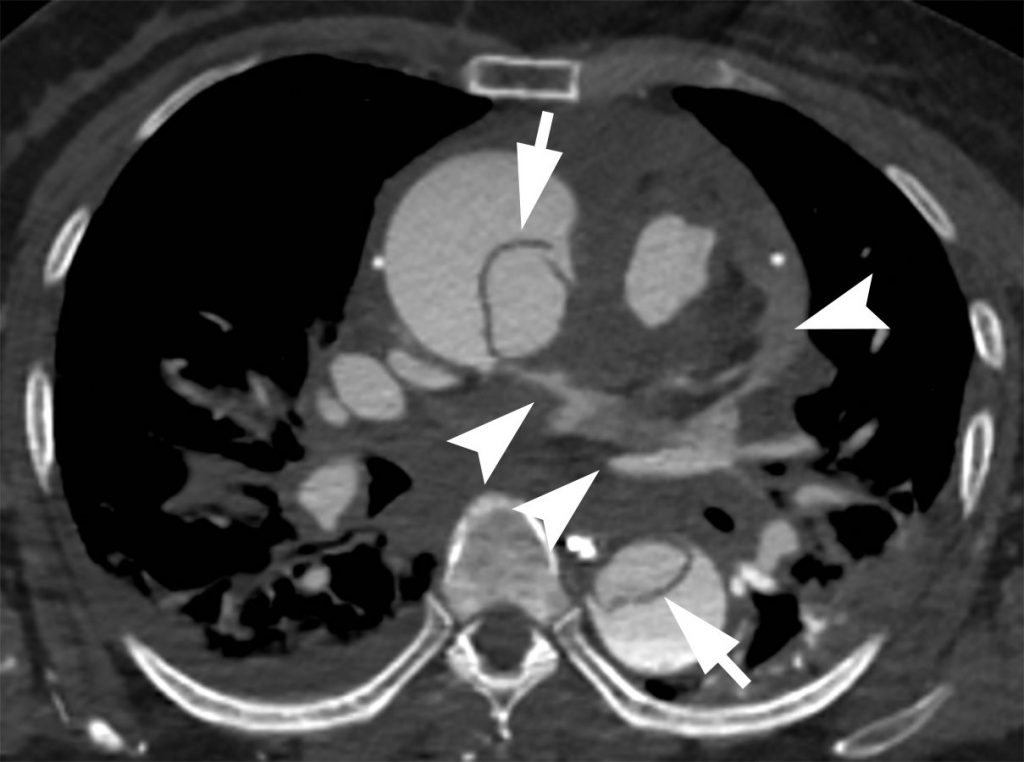
Fig. 36.9. Flap intimal de l’aorte ascendante et de l’aorte thoracique descendante (flèches) en rapport avec une dissection aortique de type A compliquée d’une rupture péricardique (têtes de flèche) et d’un hémopéricarde.
Source : CERF, CNEBMN, 2022.
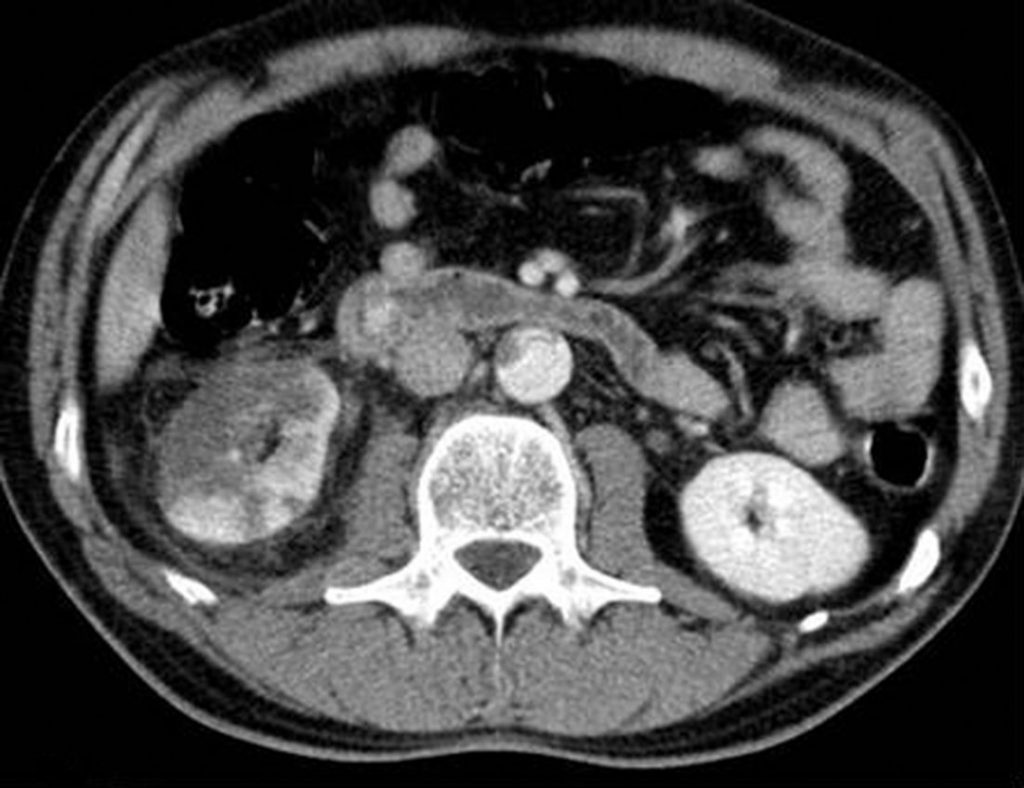
Fig. 36.10. Coupe abdominale montrant une ischémie du rein droit sous la forme d’une zone parenchymateuse étendue non rehaussée par l’injection de produit de contraste iodé.
Source : CERF, CNEBMN, 2022.
Rupture de l’isthme aortique
I. Généralités
La rupture de l’isthme correspond à une lacération de la paroi aortique thoracique secondaire à un traumatisme de haute célérité s’accompagnant d’une brutale décélération ou d’un écrasement du thorax.
Elle associe une rupture pariétale incomplète (dissection intimale, hématome pariétal ou dissection retenue par l’adventice [faux anévrisme]) ou complète (hémorragie active) associée à un hémomédiastin.
Son pronostic est gravissime puisqu’il y a seulement 20 % de survie initiale et 2 % de survie spontanée à 2 mois. Au-delà, elle peut entraîner la formation d’un faux anévrisme aortique chronique post-traumatique.
Dès lors que le diagnostic est évoqué, le patient doit être adressé en urgence vers un centre chirurgical si son état le permet.
II. Stratégie d’exploration en imagerie
A. Diagnostic
L’angioscanner thoracique est l’examen clé du diagnostic qui doit être réalisé devant toute suspicion de traumatisme thoracique grave.
Sa réalisation ne doit pas retarder une prise en charge thérapeutique urgente.
La radiographie thoracique peut évoquer le diagnostic mais sa lecture est souvent difficile et sa sensibilité est très faible. Une radiographie thoracique normale n’élimine pas le diagnostic.
L’échographie transœsophagienne peut montrer des images similaires mais n’est réalisée en urgence qu’en l’absence d’accès possible au scanner.
L’angio-IRM peut montrer des images similaires mais n’est éventuellement proposée, en substitution à l’angioscanner, qu’à distance du traumatisme.
B. Radiologie interventionnelle
Actuellement, le traitement repose en première intention sur la mise en place, par voie endovasculaire par un abord artériel fémoral, d’une endoprothèse couverte, ou stent-graft, que l’on va déployer dans l’aorte thoracique pour « recouvrir » la lésion de l’isthme aortique. Le premier temps de la pose est l’angiographie diagnostique pour mesurer le diamètre de l’aorte (si le patient n’a pas eu de scanner au préalable).
III. Sémiologie
La radiographie thoracique est hautement suggestive quand elle montre un élargissement du médiastin de plus de 8 cm lié à l’hémomédiastin et un effacement des contours de l’aorte qui deviennent flous (figure 36.11).
Sur l’angioscanner thoracique, on peut mettre en évidence :
- un flap intimal de dissection localisé à la région isthmique ;
- un hématome de la paroi aortique réduisant la lumière et induisant une hypoperfusion en aval ;
- un faux anévrisme aortique sous la forme d’une dilatation localisée de l’aorte (figure 36.12) ;
- une rupture aortique complète avec un saignement actif.
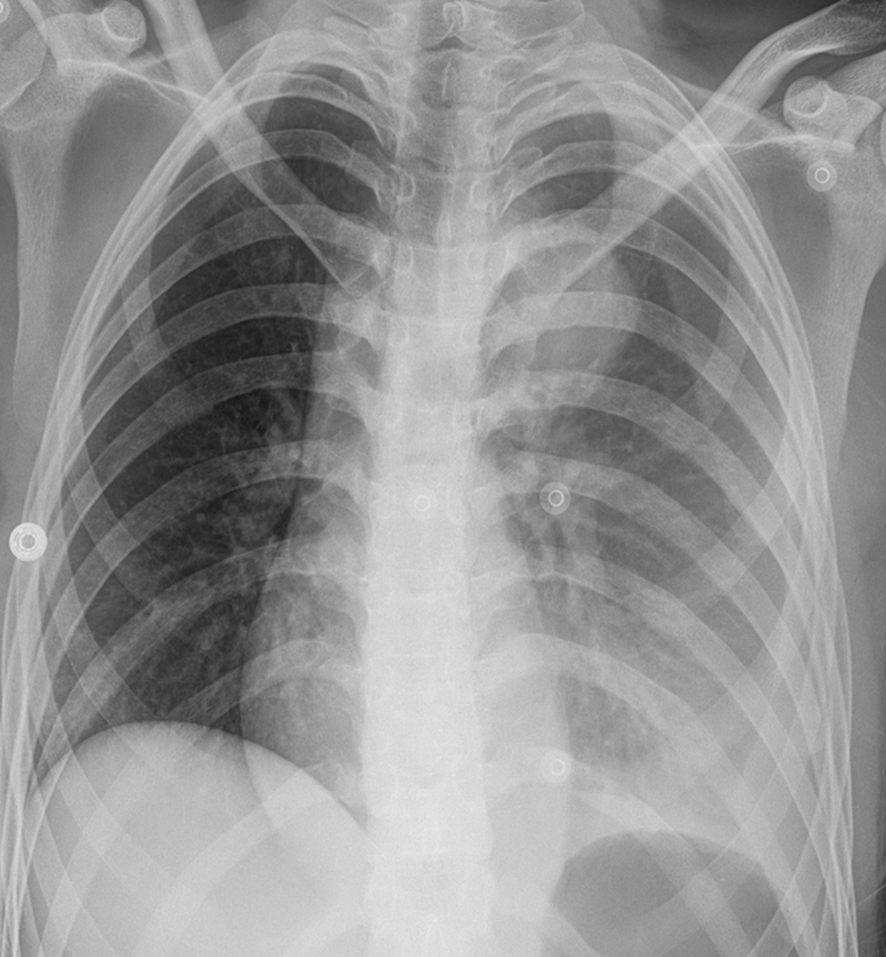
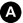
Fig. 36.11. Radiographie thoracique montrant un élargissement du médiastin lié à l’hémomédiastin et un effacement flou des contours de l’aorte.
Source : CERF, CNEBMN, 2022.
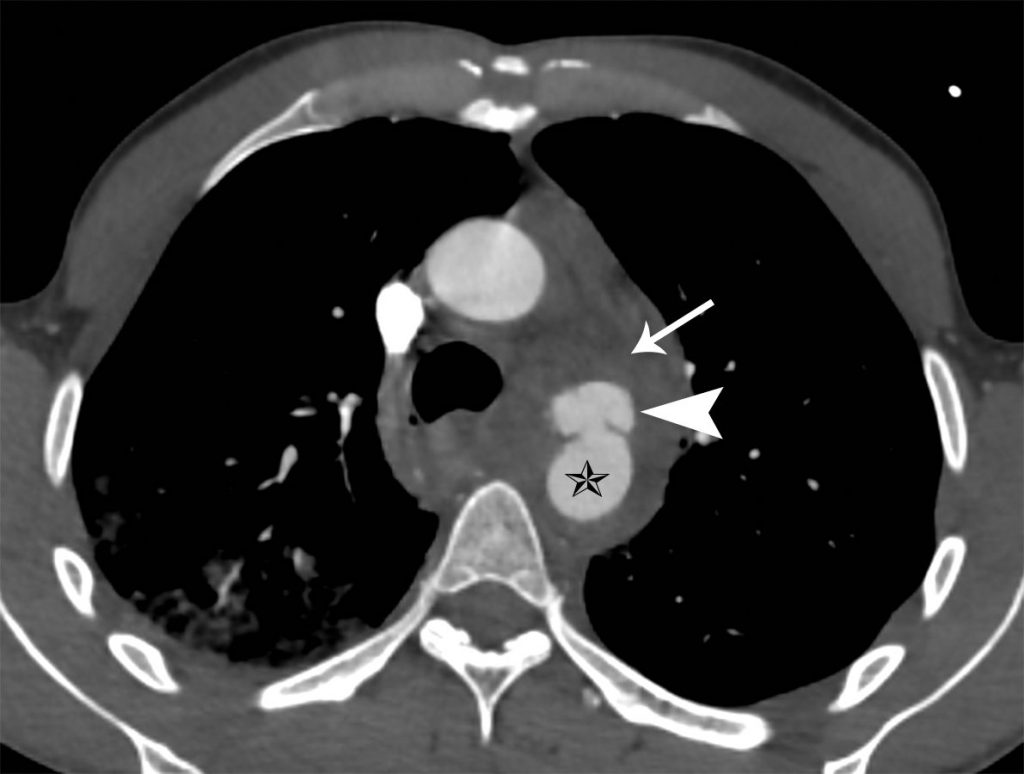
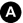
Fig. 36.12. Angioscanner thoracique montrant la lumière aortique de l’isthme (étoile) déformée à cause de la dissection localisée avec développement d’un faux anévrisme (tête de flèche) et d’un hémomédiastin (flèche).
Source : CERF, CNEBMN, 2022.
Points clés
- Le diagnostic de lésion aortique isthmique repose sur l’angioscanner thoracique devant une image de dissection localisée à l’isthme et un hémomédiastin.
- Le traitement endovasculaire est un traitement de choix de première intention.