Plan de chapitre
ITEM 44 – Tuméfaction pelvienne chez la femme
I. Généralités
II. Stratégie d’exploration en imagerie
III. Caractéristiques macroscopiques principales des masses pelviennes
IV. Exemples d’imagerie
– A. Fibrome utérin
– B. Prolapsus
– C. Kyste ovarien
Situations de départ
- 3 Distenstion abdominale
- 4 Douleur abdominale
- 8 Masse abdominale
- 16 Adénopathies unique ou multiples
- 23 Anomalie de la miction
- 98 Contraction utérine chez une femme enceinte
- 99 Douleur pelvienne
- 103 Incontinence urinaire
- 106 Masse pelvienne
- 107 Prolapsus
Item, hiérarchisation des connaissances
ITEM 44 – Tuméfaction pelvienne chez la femme
| Rang | Rubrique | Intitulé | Descriptif |
| Étiologie | Connaître les deux étiologies les plus fréquentes de tuméfaction pelvienne* | Fibrome utérin et kyste de l’ovaire | |
| Étiologie | Connaître les autres causes de tuméfaction pelvienne* | Tubaire, digestive, péritonéale | |
| Prévalence, épidémiologie | Fréquence des fibromes et des kystes ovariens bénins* | ||
| Diagnostic positif | Connaître les symptômes et les éléments de l’examen clinique liés aux fibromes* | Éléments d’orientation clinique (hémorragies, douleurs, compression, infertilité) | |
| Suivi et/ou pronostic | Connaître les principales complications des fibromes* | ||
| Étiologie | Kyste ovarien* | ||
| Diagnostic positif | Connaître les symptômes et les éléments de l’examen clinique liés aux kystes ovariens* | Éléments d’orientation clinique | |
| Étiologie | Savoir différencier kystes fonctionnel et organique* | ||
| Suivi et/ou pronostic | Connaître les principales complications des kystes ovariens* | Torsion, hémorragie, rupture, compression | |
| Identifier une urgence | Savoir évoquer une torsion d’annexe* | ||
| Examens complémentaires | Connaître les deux principaux examens radiologiques complémentaires à réaliser en cas de tuméfaction pelvienne et leur hiérarchisation (1re et deuxième intention) | Échographie et IRM | |
| Définition | Définir le prolapsus génital de la femme* | ||
| Définition | Définir les différents compartiments du prolapsus* | Cystocèle, hystérocèle ou prolapsus utérin, rectocèle, élytrocèle | |
| Diagnostic positif | Citer les diagnostics différentiels du prolapsus génital de la femme* | ||
| Prévalence, épidémiologie | Connaître la fréquence du prolapsus* | Beaucoup de prolapsus sont non symptomatiques | |
| Diagnostic positif | Connaître les signes cliniques du prolapsus* | Savoir que les signes associés génito-urinaires et sexuels ne sont pas spécifiques du prolapsus génital. Savoir que le prolapsus génital n’est a priori pas douloureux | |
I. Généralités
La découverte clinique ou fortuite d’une masse pelvienne est un événement clinique excessivement fréquent chez la femme. Il faut éliminer un contexte de grossesse par le dosage des β-hCG. En cas de positivité, l’échographie pelvienne confirmera la localisation intra- ou extra-utérine de la grossesse (figure 20.1). Les masses pelviennes sont d’origine gynécologique, essentiellement annexielles ou utérines, ou d’origine extra-gynécologique (péritonéales, digestives, urinaires, vasculaires, nerveuses). L’examen gynécologique présente des limites pour détecter et caractériser une masse pelvienne, justifiant le recours à des examens d’imagerie complémentaires.
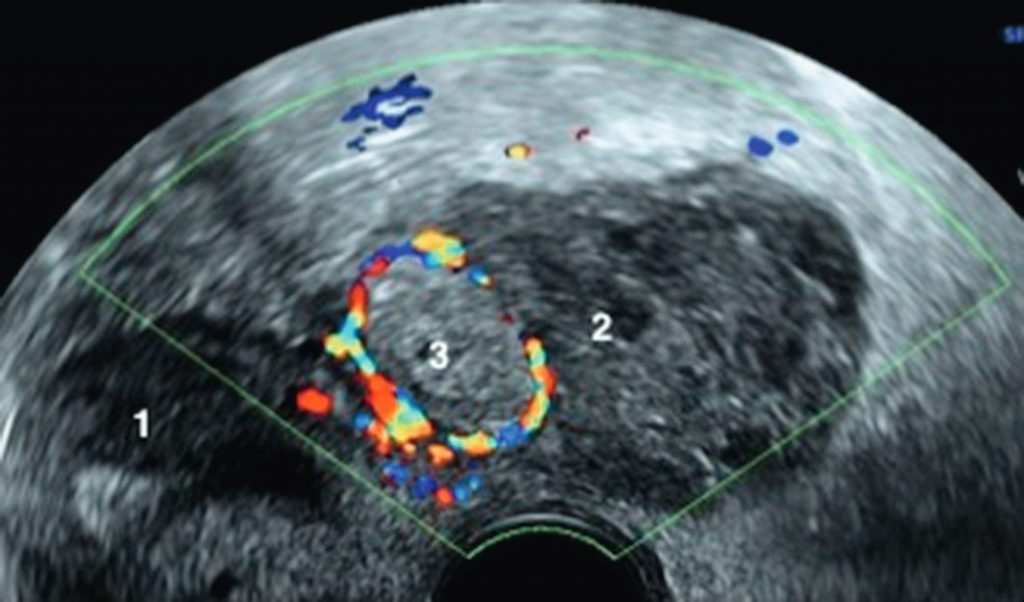
Fig. 20.1 Coupe axiale d’échographie pelvienne, chez une femme de 26 ans, présentant des douleurs pelviennes gauches, β-hCG à 1 800 UI.
1. Utérus. 2. Ovaire gauche. 3. Grossesse extra-utérine (latéro-utérine gauche) avec vascularisation périphérique au doppler couleur.
Source : CERF, CNEBMN, 2022.
II. Stratégie d’exploration en imagerie

L’échographie pelvienne (sus-pubienne et endovaginale) est la technique de première intention pour détecter et caractériser une masse pelvienne. Une étude morphologique 2D, éventuellement 3D, combinée à une étude doppler couleur sera réalisée pour une caractérisation optimale.
L’IRM pelvienne procure une meilleure caractérisation tissulaire que l’échographie-doppler ou le scanner en cas de masse indéterminée ou complexe en échographie.
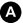
La principale étiologie annexielle est le kyste fonctionnel (figures 20.2 et 20.3).
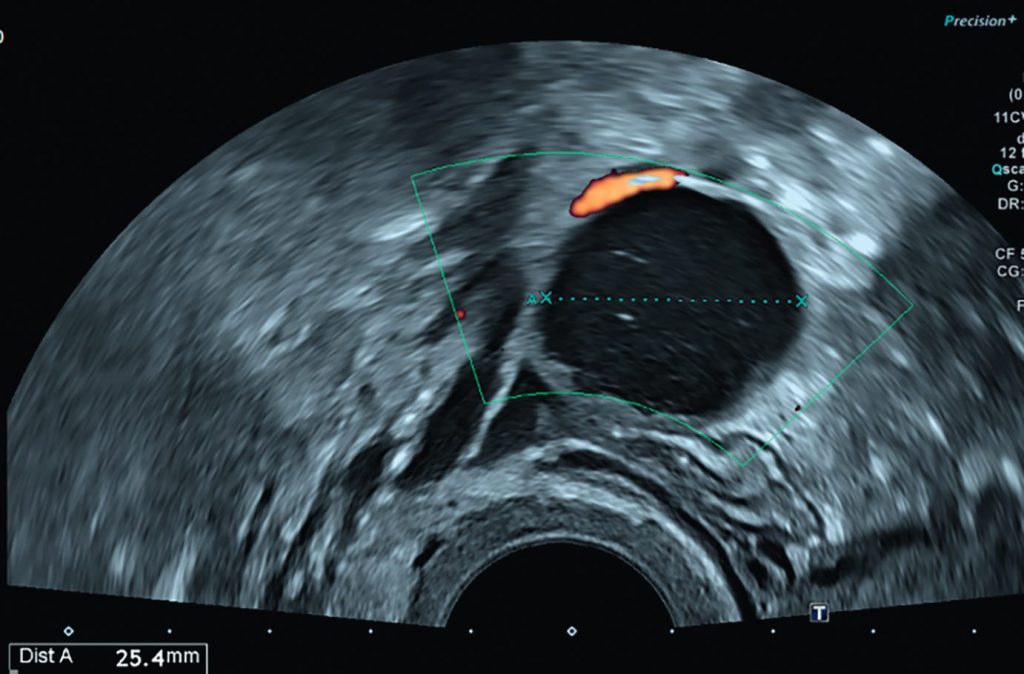

Fig. 20.2 Formation kystique uniloculaire pure ovarienne droite de paroi fine, anéchogène, avec un aspect en « filet de pêche », sans hypervascularisation au doppler couleur en faveur d’un kyste fonctionnel hémorragique.
Source : CERF, CNEBMN, 2022.
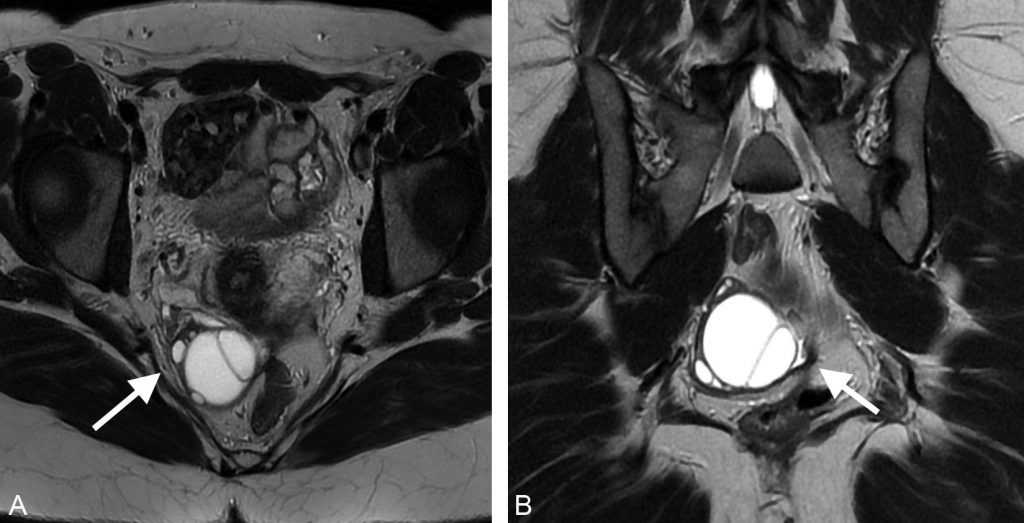

Fig. 20.3 Coupe axiale (A) et coronale (B) d’IRM pelvienne en séquence T2 chez une patiente de 28 ans présentant des douleurs pelviennes latéralisée à droite.
On retrouve une formation uniloculaire pure développée aux dépens de l’ovaire droit de paroi fine, en franc hypersignal T2 liquidien, sans végétation ni portion tissulaire, faisant évoquer fortement un kyste fonctionnel de l’ovaire.
Source : CERF, CNEBMN, 2022.

L’IRM permettra dans la grande majorité des cas de différencier les lésions bénignes des lésions malignes en particulier ovariennes et utérines.
Le scanner ne présente plus d’indication pour la caractérisation d’une masse pelvienne, en dehors d’une suspicion échographique de tératome (figures 20.4 et 20.5). Il reste utile dans le contexte de l’urgence, en particulier pour éliminer une torsion annexielle surajoutée ou dans un contexte septique abdominopelvien ou dans le bilan d’extension d’une masse ovarienne suspecte.
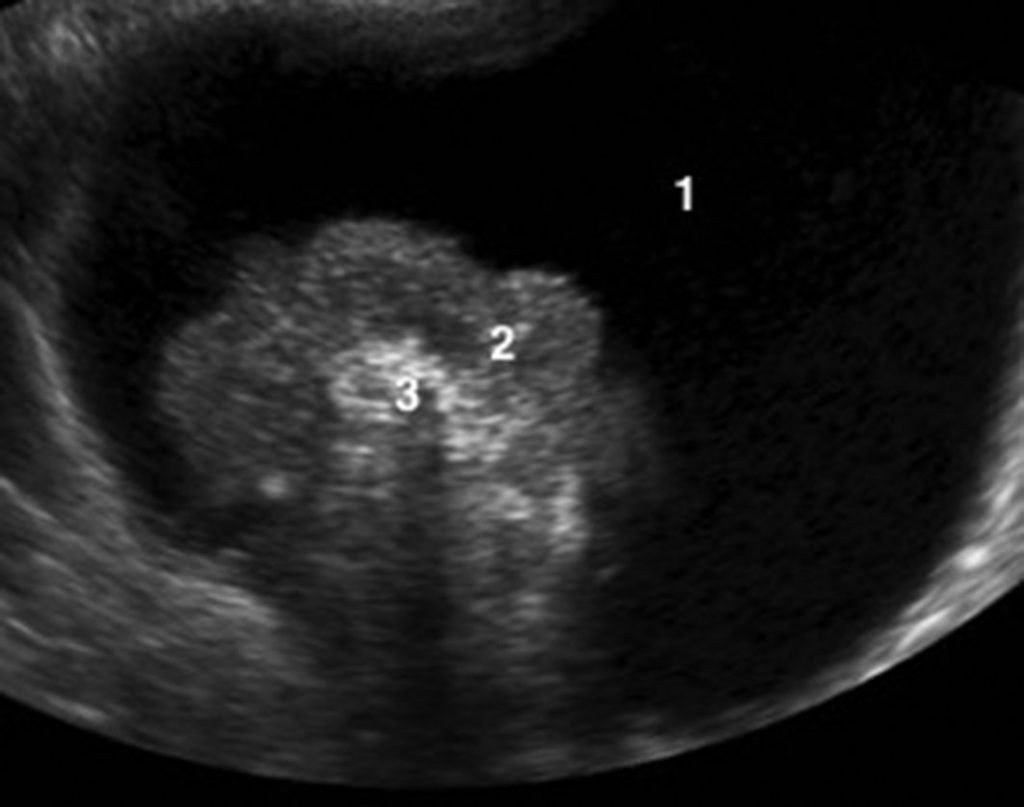

Fig. 20.4 Coupe axiale d’échographie pelvienne centrée sur un kyste ovarien droit mixte (liquidien et solide).
1. Portion liquidienne anéchogène. 2. Portion solide. 3. Calcification hyperéchogène atténuante.
Source : CERF, CNEBMN, 2022.
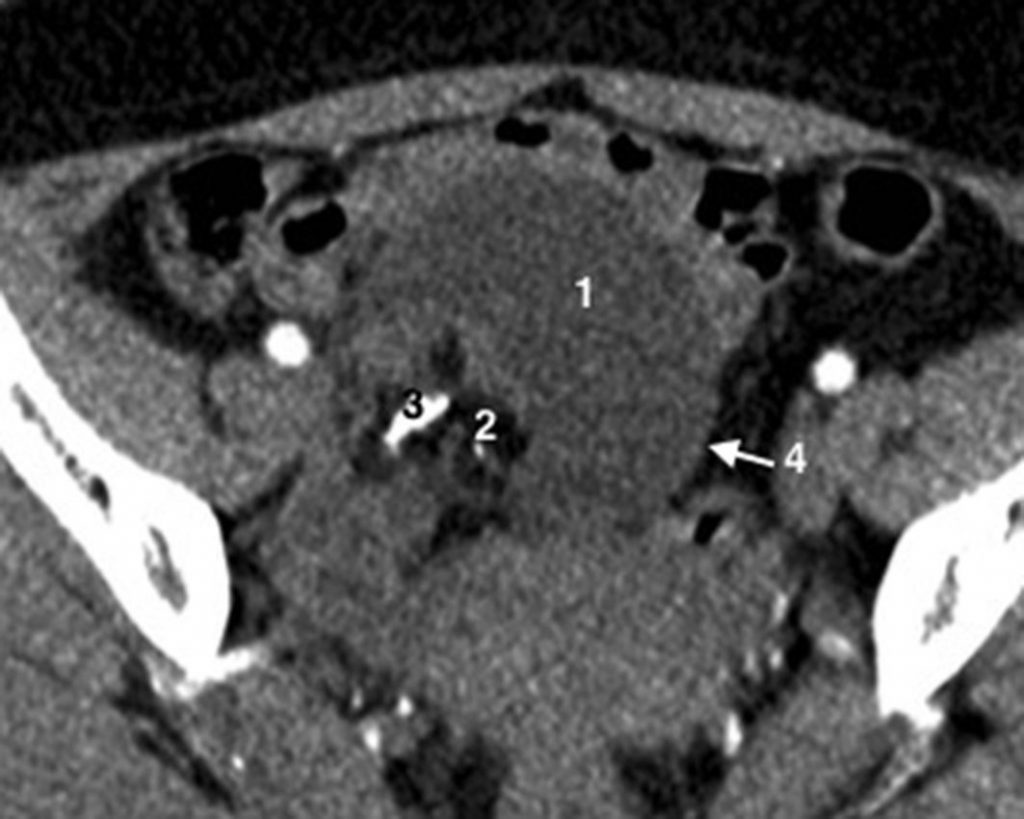

Fig. 20.5 Coupe axiale de scanner pelvien sans injection centrée sur un kyste ovarien droit mixte (liquidien et solide), même patiente que la figure 25.4.
1. Portion liquidienne. 2. Portion hypodense graisseuse. 3. Calcification. 4. Paroi du kyste.
Source : CERF, CNEBMN, 2022.
III. Caractéristiques macroscopiques principales des masses pelviennes
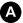
La topographie lésionnelle, les rapports anatomiques et l’aspect macroscopique permettent de regrouper les lésions en plusieurs catégories (tableau 20.1 ; ne sont mentionnées que les tumeurs les plus communément décrites). On retiendra cependant que les myomes utérins (figure 20.6) (très fréquents et bénins, à la différence du sarcome utérin) et les kystes ovariens (figure 20.7) (bénin, borderline, ou malin) sont les plus fréquents en gynécologie. Pour les pathologies non gynécologiques, il faut penser au fécalome et au globe vésical, dont le diagnostic est clinique.
Tableau 20.1 ![]() Classification des principales masses pelviennes selon leur aspect et leur origine.
Classification des principales masses pelviennes selon leur aspect et leur origine.
| Origine | |||||
| Ovarienne | Tubaire | Péritonéale | Utérine | Autre | |
| Aspect kystique | Fonctionnelle Organique (épithéliale bénigne) | Hydrosalpinx (tubulé) | Pseudokyste péritonéal (moulé sur les organes de voisinage) | – | – |
| Aspect solide | Fibrome ovarien Métastases Germinales Stromales et des cordons sexuels | – | Carcinose | Myome sous-séreux pédiculé Utérus poly-myomateux | Digestive (GIST) Neurogène (neurofibrome) Adénopathie |
| Aspect mixte (solide + kystique) | Germinales (tératome) Épithéliale (maligne) Métastases (primitif digestif) | Grossesse extra-utérine | – | – | – |
(Source : CERF, CNEBMN, 2022.)
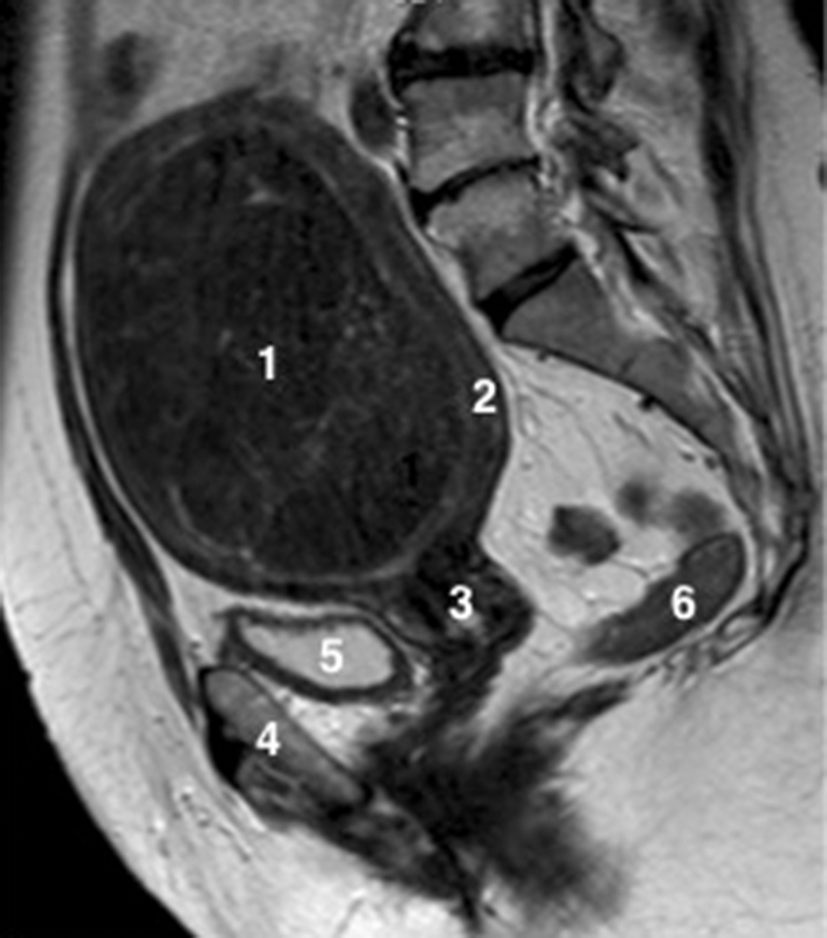

Fig. 20.6 Coupe sagittale d’IRM pelvienne chez une patiente présentant cliniquement une masse pelvienne associée à des ménorragies.
1. Volumineux myome intracavitaire en hyposignal T2, fibreux non suspect. 2. Myomètre refoulé par le myome. 3. Col utérin. 4. Pubis. 5. Vessie. 6. Rectum.
Source : CERF, CNEBMN, 2022.
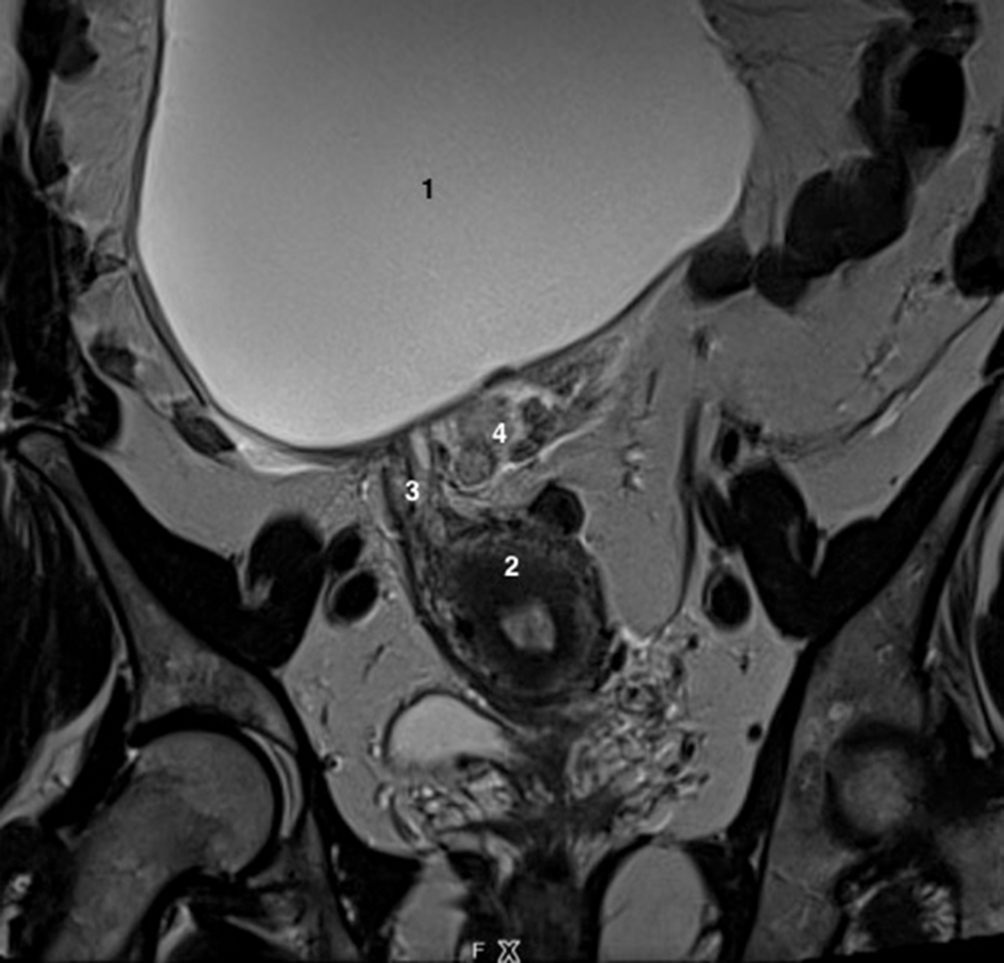

Fig. 20.7 Coupe coronale d’IRM pelvienne chez une patiente présentant cliniquement une masse pelvienne et des douleurs pelviennes aiguës.
1. Kyste ovarien droit en hypersignal T2 liquidien. 2. Utérus. 3. Trompe droite épaissie et œdématiée, « allongée », en hypersignal T2. 4. Trompe droite de « forme ronde en coupe » témoignant d’un enroulement de celle-ci associé à un épanchement péri-annexiel.
Source : CERF, CNEBMN, 2022.
IV. Exemples d’imagerie
A. Fibrome utérin

En général, le diagnostic de fibrome est fait à l’examen gynécologique et fortement suspecté après une échographie abdominopelvienne (échographie par voie abdominale et par voie transvaginale). En complément, l’échosonographie, consistant à l’injection intra-utérine de sérum physiologique, peut être utile pour mieux visualiser les images endocavitaires. Le diagnostic peut être confirmé par une hystéroscopie permettant l’examen fonctionnel de l’endomètre et la réalisation de biopsies guidées. L’IRM pelvienne avec injection (figure 20.8) permet aussi de confirmer le diagnostic et d’éliminer d’autres pathologies (adénomyose, sarcome), sans pouvoir toutefois exclure avec certitude le diagnostic de sarcome. Elle permet aussi de repérer les caractéristiques du ou des fibrome(s) utiles pour la décision thérapeutique, telles que leur taille, nombre, localisation et classification FIGO.
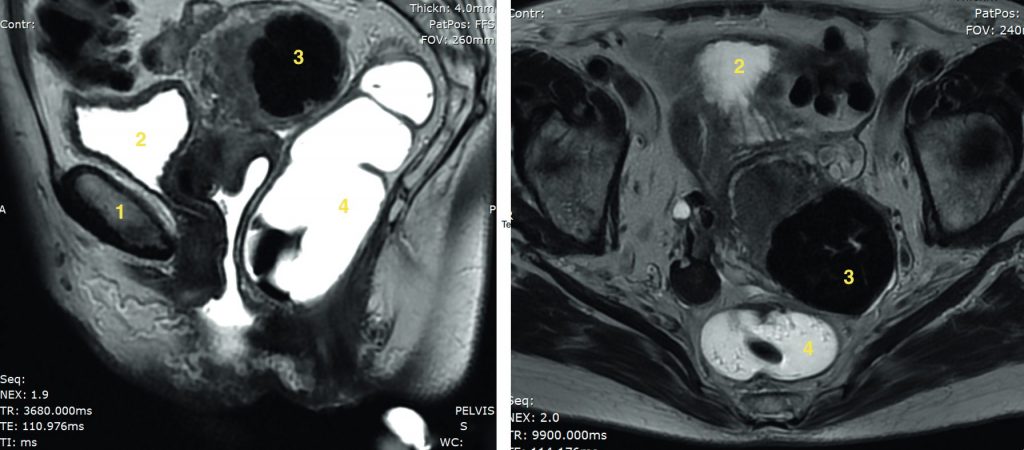

Fig. 20.8 IRM pelvienne. Patiente de 46 ans présentant des douleurs pelviennes latéralisées.
1. Pubis. 2. Vessie. 3. Fibrome sous-séreux corporéal latéralisé à gauche en franc hyposignal T2, en remaniement hyalin. 4. Rectum.
Source : CERF, CNEBMN, 2022.
B. Prolapsus
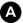
Le symptôme le plus spécifique d’un prolapsus est la boule vaginale perçue ou ressentie par la patiente.

Le prolapsus génital de la femme peut se définir comme une hernie dans la cavité vaginale (colpocèle), dans laquelle s’engagent un ou plusieurs éléments du contenu pelvien.
Les organes des trois compartiments du pelvis peuvent être concernés :
- en avant, colpocèle antérieure (dite cystocèle car contient la vessie) ;
- compartiment moyen ou apical : l’utérus (hystéroptose) ou le fond vaginal (prolapsus du fond vaginal) si la patiente a eu une ablation de l’utérus ;
- en arrière, colpocèle postérieure, qui peut contenir le rectum (rectocèle) ou le cul-de-sac péritonéal (élytrocèle) avec le contenu abdominal (intestin, omentum).
Le prolapsus rectal est à différencier de la rectocèle : il correspond à l’extériorisation d’une partie du rectum par l’orifice anal.
L’IRM dynamique (figure 20.9) permet de faire le bilan complet d’un prolapsus complexe avant de décider de la chirurgie à proposer, et également de chercher une éventuelle cause anatomique à des anomalies d’évacuation ou de rétention du contenu intestinal.

Fig. 20.9 Patiente de 65 ans, présentant une boule vaginale à l’effort. Une IRM pelvienne est réalisée. La séquence rapide sagittale T2 retrouve une hystérocèle de grade III (H) et une cystocèle de grade III (C).Il n’existe pas de rectocèle.
Source : CERF, CNEBMN, 2022.
C. Kyste ovarien
Un kyste fonctionnel (figure 20.10A) est en général une formation kystique uniloculaire pure ou plurilocaculaire avec une cloison fine, sans végétation, ni portion tissulaire intra- ou extrakystique, de paroi fine. Une hypervascularisation périphérique au doppler couleur est possible.
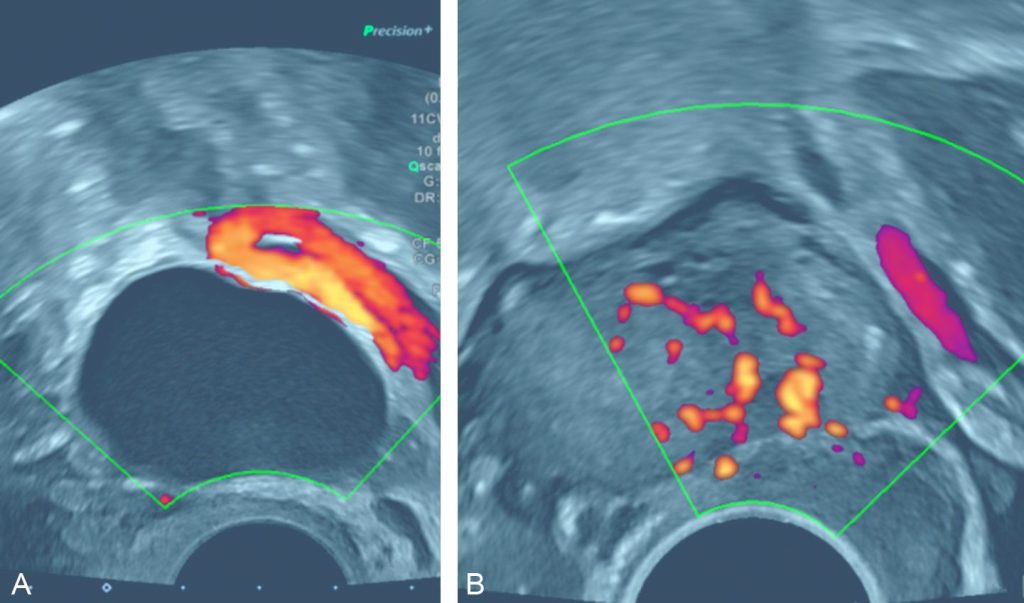

Fig. 20.10 A. Patiente de 45 ans présentant une douleur pelvienne latéralisée à gauche. B. Patiente de 21 ans, nulligeste, découverte fortuite d’une masse ovarienne sur l’échographie réalisée pour contrôle de la pose d’un dispositif utérin.
A. L’échographie endovaginale retrouve une formation kystique uniloculaire pure ovarienne gauche, de parois fines, sans portion tissulaire, ni hypervascularisation au doppler couleur. Le contrôle échographique réalisé à 3 mois ne met plus en évidence la formation kystique, ce qui confirme son caractère fonctionnel. B. L’échographie endovaginale met en évidence une formation hyperéchogène ovarienne gauche avec hypervascularisation au doppler couleur, témoignant d’une volumineuse portion tissulaire, en faveur d’un kyste organique.
Source : CERF, CNEBMN, 2022.
Un kyste organique (figure 20.10B) peut se présenter par une formation kystique uniloculaire pure persistante depuis plus de 3 mois. Un kyste organique doit être évoqué en première hypothèse lorsqu’il existe une végétation, une portion tissulaire ou encore si les cloisons sont épaisses et irrégulières.
Points clés
- La découverte clinique ou fortuite d’une masse pelvienne est très fréquente chez la femme.
- L’échographie pelvienne (sus-pubienne et endovaginale) est l’examen de première intention pour détecter et caractériser une masse pelvienne.
- L’IRM permet dans la grande majorité des cas de différencier les lésions bénignes des lésions malignes, en particulier ovariennes et utérines.